题目内容
12.化学是以实验为基础的科学.根据如图所示的实验,请回答: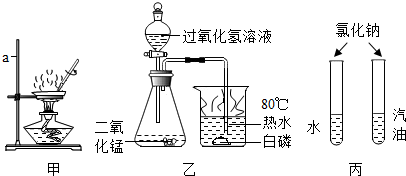
(1)甲是蒸发溶液的实验,其中玻璃棒的作用是防止局部温度过高,造成液滴飞溅.
(2)乙是探究燃烧条件的实验.打开分液漏斗的活塞前,白磷不燃烧,而打开活塞后,白磷在水中燃烧.比较打开活塞前后的现象,证明白磷燃烧需要氧气;烧杯中80℃的热水的作用是隔绝氧气、使白磷的温度达到着火点.写出锥形瓶中反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;烧杯中白磷燃烧的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(3)丙是一组对比实验,实验目的是比较同种溶质在不同溶剂中的溶解性.
分析 (1)根据蒸发过程中玻璃棒的作用进行分析;
(2)根据燃烧的条件进行分析解答;
(3)根据物质的溶解于溶剂的种类有关进行分析解答即可.
解答 解:(1)用玻璃棒不断搅拌的目的是使液体受热均匀,防止局部温度过高,造成液滴飞溅,
故答案为:防止局部温度过高,造成液滴飞溅;
(2)打开分液漏斗的活塞前,没有氧气,白磷不燃烧,而打开后,过氧化氢在二氧化锰的催化作用下产生了氧气,白磷燃烧,说明燃烧需要氧气;烧杯中的水一方面可以隔绝氧气,另一方面使白磷的温度达到着火点,制氧气的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;白磷燃烧生成了五氧化二磷,反应的化学方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
故答案为:氧气;隔绝氧气、使白磷的温度达到着火点;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(3)丙实验是将氯化钠加入等量的水和汽油中,该实验是想比较同种溶质在不同溶剂中的溶解性,
故答案为:比较同种溶质在不同溶剂中的溶解性.
点评 本题考查了对常见实验的解释,完成此题,可以依据已有的知识结合题干提供的信息进行.

练习册系列答案
相关题目
2.央视报道“全国多地相继出现了“假干粉灭火器”,干粉灭火器中灭火剂的主要成分是碳酸氢钠,而假干粉灭火器是用面粉做灭火剂,兴趣小组同学想了解学校干粉灭火器的灭火剂是否为报道中的“假干粉”.设计了以下探究一:甲、乙同学分别用物理方法和化学方法设计方案,进行如下实验:
乙同学设计方案中发生反应的化学方程式为NaHCO3+HCl═NaCl+H2O+CO2↑
探究二:小组同学利用灭火器进行实验后,发现可燃物表面有白色粉末残留.为了解白色粉末的主要成分,继续以下探究:
【查阅资料】1、碳酸钠受热不分解.
2、碳酸氢钠溶解吸收热量;碳酸钠溶解放出热量.
【提出猜想】猜想1:残留主要成分是碳酸钠;猜想2:残留主要成分是碳酸氢钠和碳酸钠
【设计方案】小组同学设计的下列实验方案中,错误的是B(填序号)
A、加热残留物质将产生的气体通入澄清的石灰水中,若观察到澄清石灰水变浑浊,则猜想2正确.
B、将残留物溶于水,若有放热现象,则猜想1正确
C、将残留物溶于水,加过量氯化钙溶液静置,取上层清液加稀盐酸,若产生气泡,则猜想2正确
【反思评价】设计实验方案要思维缜密,考虑周全.用化学知识解释上述错误方案存在的主要问题无论残留物中是否含有碳酸氢钠,固体溶解后,溶液温度都可能升高.
| 实验步骤 | 实验现象 | 实验结论 | |
| 甲 | 取少量灭火剂于试管中,加入一定量的水 | 粉末逐渐溶解 | 该灭火剂不属于报道中的“假干粉” |
| 乙 | 取少量灭火剂于试管中,加入一定量的稀盐酸 | 有气泡产生 |
探究二:小组同学利用灭火器进行实验后,发现可燃物表面有白色粉末残留.为了解白色粉末的主要成分,继续以下探究:
【查阅资料】1、碳酸钠受热不分解.
2、碳酸氢钠溶解吸收热量;碳酸钠溶解放出热量.
【提出猜想】猜想1:残留主要成分是碳酸钠;猜想2:残留主要成分是碳酸氢钠和碳酸钠
【设计方案】小组同学设计的下列实验方案中,错误的是B(填序号)
A、加热残留物质将产生的气体通入澄清的石灰水中,若观察到澄清石灰水变浑浊,则猜想2正确.
B、将残留物溶于水,若有放热现象,则猜想1正确
C、将残留物溶于水,加过量氯化钙溶液静置,取上层清液加稀盐酸,若产生气泡,则猜想2正确
【反思评价】设计实验方案要思维缜密,考虑周全.用化学知识解释上述错误方案存在的主要问题无论残留物中是否含有碳酸氢钠,固体溶解后,溶液温度都可能升高.
3.下列物质的用途主要是由其化学性质决定的是( )
| A. | 干冰可用于人工降雨 | B. | 生铁制成铁锅 | ||
| C. | 铜丝可用来制作导线 | D. | 氢气可做清洁燃料 |
20.下列对实验操作或现象的分析不正确的是( )
| A. | 用灯帽盖灭酒精灯,是为了降低可燃物的温度 | |
| B. | 用扇子扇灭烛火,是为了降温使温度低于蜡烛的着火点 | |
| C. | 用水湿润玻璃管口,是为了增强玻璃管与乳胶管间的润滑 | |
| D. | 在做用酸碱中和反应的实验时,酚酞试液滴入碱溶液中,是为了指示酸与碱发生化学的反应. |
7. 如图是在一定量氢氧化钠溶液中不断加入盐酸的曲线图,纵坐标能表示的意义是( )
如图是在一定量氢氧化钠溶液中不断加入盐酸的曲线图,纵坐标能表示的意义是( )
 如图是在一定量氢氧化钠溶液中不断加入盐酸的曲线图,纵坐标能表示的意义是( )
如图是在一定量氢氧化钠溶液中不断加入盐酸的曲线图,纵坐标能表示的意义是( )| A. | 氢氧化钠的质量 | B. | 生成氯化钠的质量 | ||
| C. | 溶液中水的质量 | D. | 溶液的PH值 |
17.下列物质排放到空气中,不会造成大气污染的是( )
| A. | SO2 | B. | NO2 | C. | CO | D. | CO2 |
1.下列事实可用金属活动性顺序加以解释的是( )
| A. | 铁的导热性能比铝的好 | B. | 铝制品比铁制品更耐用 | ||
| C. | 常用铜、铝而不用银做导线 | D. | 不能用铁制容器配制硫酸铜溶液 |
2.下列过程发生了物理变化的是( )
| A. | 木柴燃烧 | B. | 葡萄酿酒 | C. | 冰雪融化 | D. | 生石灰吸水放热 |