题目内容
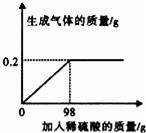
为测定某锌和铜的混合物样品中锌的含量,现将10g样品置于烧杯中,加入一定质量的稀硫酸(样中的铜不与稀硫酸反应).所加稀硫酸与生成气体的质量关系如图所示.计算该样品中铜的质量分数.

【考点】根据化学反应方程式的计算.
【专题】有关化学方程式的计算.
【分析】据图中数据可以判断生成氢气的质量;根据氢气的质量可以计算锌的质量,进一步可以计算样品中铜的质量分数.
【解答】解:生成氢气的质量是0.2g;
设锌的质量为x,
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.2g
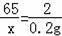

x=6.5g
样品中铜的质量分数为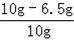
 ×100%=35%
×100%=35%
答:该样品中铜的质量分数为35%.
【点评】本题主要考查学生运用化学方程式进行计算和推断的能力,比较简单,计算时要注意规范性和准确性.

练习册系列答案
相关题目
下表列出了除去物质中所含少量杂质的方法,其中错误的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CO2 | CO | 点燃 |
| B | CaCl2溶液 | HCl | 加入过量CaCO3,过滤 |
| C | H2 | CO2 | 通入足量的氢氧化钠溶液 |
| D | CuO | Cu | 空气中加热 |
A.A B.B C.C D.D