题目内容
【题目】没有水就没有生命。下列有关水的说法正确的是
A.将硬水过滤或加入明矾,都可以得到软水
B.自然界中的水循环说明水分子在不断运动
C.“氢气燃烧生成水”不能说明水由氢元素和氧元素组成
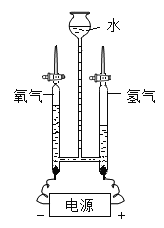
D.电解水产生气体的同时,漏斗中的液面会不断下降
【答案】B
【解析】
A、硬水中溶有较多的可溶性钙、镁化合物,过滤只能除去硬水中的不溶性杂质,无法除去可溶性钙、镁化合物;明矾是絮凝剂,具有吸附沉降的作用,向硬水中加入明矾,不能使钙、镁离子沉淀,故A错误;
B、自然界的水循环是水分子不断运动的结果,故B正确;
C、氢气燃烧生成水时,氢气中的氢元素、氧气中的氧元素都进入了水中,说明水是由氢元素和氧元素组成的,故C错误;
D、电解水时,与电源正负极相连的两个集气管内不断生成气体;分解掉很少的水,生成的氢气或氧气所占的体积都很大,这样就把左右两个集气管里的水不断压入漏斗中,使漏斗中的液面不断升高,故D错误。故选B。

练习册系列答案
相关题目