题目内容
11.阅读下面科普短文.在刑侦破案时,凶案现场若有血迹,不管经过何种方式的清除,只要喷洒鲁米诺试剂并在黑暗环境下观察,原沾有血迹的地方就会发出蓝紫色的荧光.
鲁米诺试剂是鲁米诺与过氧化氢、氢氧化钠溶液的混合物,主要用于现代刑侦的血液检测.
鲁米诺(luminol)的化学名称为3-氨基邻苯二甲酰肼,化学式为C8H7N3O2.它是一种人工合成的有机物,常温下是黄色粉末,其水溶液显强酸性,对眼睛、皮肤、呼吸道有一定刺激作用.
鲁米诺在1853年被合成出来.1928年,化学家首次发现这种化合物有一个奇妙的特性,当它被氧化时能发出蓝光.几年以后,就有人想到利用这种特性去检测血迹.血液中含有血红蛋白,血红蛋白含有亚铁,而亚铁能催化过氧化氢的分解,让过氧化氢变成水和氧气,氧气再氧化鲁米诺让它发光.
这种检测方法极为灵敏,能检测只有百万分之一含量的血,即使滴一小滴血到一大缸水中也能被检测出来,由此可知犯罪分子是多么难以把现场血迹清洗干净了.
依据文章内容,回答下列问题:
(1)鲁米诺含有四种元素.
(2)鲁米诺的物理性质黄色粉末,可溶于水.
(3)鲁米诺发光过程中主要发生化学变化(填“物理变化”或“化学变化”).
(4)血红蛋白使过氧化氢产生氧气的原因是(用化学方程式表示)2H2O2$\frac{\underline{\;血红蛋白\;}}{\;}$2H2O+O2↑.
(5)在鲁米诺试剂中,鲁米诺分子结构会发生改变,原因是鲁米诺在溶液中呈酸性,而鲁米诺试剂中含有氢氧化钠,二者发生反应,使鲁米诺分子结构发生改变.
分析 (1)根据化学式判断物质的元素组成;
(2)根据物理性质的定义进行解答;
(3)根据化学变化的定义进行解答;
(4)根据化学方程式的书写规则进行解答;
(5)根据鲁米诺在溶液中呈酸性,以及鲁米诺试剂的成分进行解答;
解答 解:(1)根据鲁米诺的化学式C8H7N3O2可知,其是由碳、氢、氮、氧四种元素组成的;
(2)物理性质就是不需要经过化学变化就能表现出来的性质,由题意可知,鲁米诺的物理性质为:黄色粉末,可溶于水;
(3)鲁米诺被氧化是可发光,被氧化的过程是一个化学变化的过程,故发光过程中主要发生在化学变化;
(4)根据题意可知,过氧化氢在血红蛋白的催化作用下分解为水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;血红蛋白\;}}{\;}$2H2O+O2↑;
(5)在鲁米诺试剂中,鲁米诺分子结构会发生改变,原因是鲁米诺在溶液中呈酸性,而鲁米诺试剂中含有氢氧化钠,二者发生反应,使鲁米诺分子结构发生改变;
故答案为:(1)四; (2)黄色粉末,可溶于水; (3)化学变化;(4)2H2O2$\frac{\underline{\;血红蛋白\;}}{\;}$2H2O+O2↑;
(5)鲁米诺在溶液中呈酸性,而鲁米诺试剂中含有氢氧化钠,二者发生反应,使鲁米诺分子结构发生改变;
点评 本题主要考查了化学式的含义,物质性质、化学变化的定义,化学方程式的书写等知识,以及考查学生从题干中选取信息分析问题的能力.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
17.下列关于物质性质的描述中,属于化学性质的是( )
| A. | 酒精易挥发 | B. | 二氧化碳的密度比空气的密度大 | ||
| C. | 钢铁在潮湿的空气中易生锈 | D. | 食盐放入水中搅拌后变为食盐水 |
6.根据下图所示实验分析得出的结论中,不正确的是( )
| A. |  甲烷燃烧生成水 甲烷燃烧生成水 | |
| B. |  铁能在氧气中燃烧 | |
| C. |  酚酞分子不断运动,并扩散到了浓氨水中 酚酞分子不断运动,并扩散到了浓氨水中 | |
| D. |  二氧化碳的密度比空气大,不燃烧也不支持燃烧 二氧化碳的密度比空气大,不燃烧也不支持燃烧 |
16.资料表明:在不同温度下,CO可将Fe2O3还原为Fe、Fe3O4中的一种或两种.为探究温度对该反应产物的影响,进行如下实验.
【查阅资料】
Ⅰ.Fe3O4与盐酸反应,得到FeCl2和FeCl3的混合溶液
Ⅱ.用溶质质量分数一定的FeCl2和FeCl3溶液进行如下实验,为方案设计提供参考
【实验过程】
甲、乙两组同学分别用酒精灯和酒精喷灯作为热源进行CO还原Fe2O3的实验,检验得到的黑色固体的成分,完成如表实验报告.
【实验反思】
(1)结合此次探究活动,你认为下列说法正确的是abcd(填字母序号).
a.温度会影响反应的产物 b.进行CO还原Fe2O3的实验时,一定要进行尾气处理
c.KSCN溶液可用于检验FeCl3溶液 d.得到的黑色固体的质量一定小于参加反应的Fe2O3的质量
(2)乙组的实验结论有欠缺,请你分析原因若固体是Fe和Fe3O4的混合物,过量的Fe可与FeCl3反应生成FeCl2,加入KSCN溶液同样能观察到溶液无明显变化.
【查阅资料】
Ⅰ.Fe3O4与盐酸反应,得到FeCl2和FeCl3的混合溶液
Ⅱ.用溶质质量分数一定的FeCl2和FeCl3溶液进行如下实验,为方案设计提供参考
| FeCl2溶液 | FeCl3溶液 | |
| 加入Fe粉 | 无明显变化 | 溶液变成浅绿色 |
| 加KSCN溶液 | 无明显变化 | 溶液变成红色 |
甲、乙两组同学分别用酒精灯和酒精喷灯作为热源进行CO还原Fe2O3的实验,检验得到的黑色固体的成分,完成如表实验报告.
| 实验操作 | 实验现象 | 结论与解释 |
| ①取少量的黑色固体于试管中,滴加适量的稀盐酸 ②向步骤①所得的溶液中,滴加KSCN溶液 | 甲组: 固体溶解,无气泡冒出 加KSCN溶液后,溶液变成红色 | 甲组用CO还原Fe2O3反应的化学方程式是CO+3Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe3O4+CO2 |
| 乙组: 固体溶解,有气泡冒出 加KSCN溶液后,溶液颜色无明显变化 | 黑色固体的成分是Fe |
(1)结合此次探究活动,你认为下列说法正确的是abcd(填字母序号).
a.温度会影响反应的产物 b.进行CO还原Fe2O3的实验时,一定要进行尾气处理
c.KSCN溶液可用于检验FeCl3溶液 d.得到的黑色固体的质量一定小于参加反应的Fe2O3的质量
(2)乙组的实验结论有欠缺,请你分析原因若固体是Fe和Fe3O4的混合物,过量的Fe可与FeCl3反应生成FeCl2,加入KSCN溶液同样能观察到溶液无明显变化.
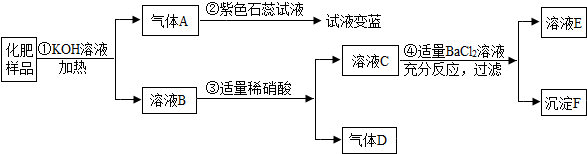
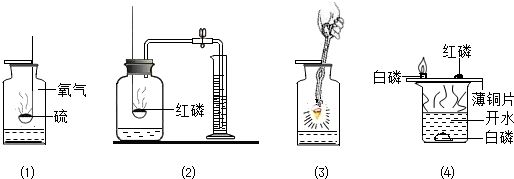
 实验室中用如下实验来研究铁、铝、铜三种金属活动顺序及其在活动顺序表中相对氢的位置.
实验室中用如下实验来研究铁、铝、铜三种金属活动顺序及其在活动顺序表中相对氢的位置.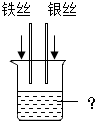 某班同学做验证铁、铜、银的金属活动性顺序的实验,用到的药品有铁丝、铜丝、银丝、稀硫酸和硫酸铜溶液.实验结束后,化学兴趣小组的同学欲对该实验的废液进行探究,请你一起参与.
某班同学做验证铁、铜、银的金属活动性顺序的实验,用到的药品有铁丝、铜丝、银丝、稀硫酸和硫酸铜溶液.实验结束后,化学兴趣小组的同学欲对该实验的废液进行探究,请你一起参与.