题目内容
9.向一定量的碳酸钠溶液中加入105g氯化钙溶液,恰好完全反应,过滤,得到5g白色沉淀和200g滤液,计算:(1)参加反应的碳酸钠的质量;
(2)碳酸钠溶液中溶质的质量分数.
分析 据质量守恒定律可以求算出碳酸钠溶液的质量;根据氯化钙和碳酸钠反应的化学方程式结合生成的沉淀质量可以计算才固体混合物中碳酸钠的质量.
解答 解:(1)设参加反应的碳酸钠的质量为x,
CaCl2+Na2CO3═CaCO3↓+2NaCl
106 100
x 5g
$\frac{106}{x}$=$\frac{100}{5g}$
x=5.3g
(2)碳酸钠溶液中溶质的质量分数为$\frac{5.3g}{200g+5g-105g}$×100%=5.3%
答:参加反应的碳酸钠的质量为5.3g.
碳酸钠溶液中溶质的质量分数为5.3%.
点评 要想解答好这类题目,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.

练习册系列答案
相关题目
19.除去各物质中所含少量杂质,所选用的试剂及操作方法均正确的是( )
| 选项 | 物质(括号内为杂质) | 试 剂 | 操作方法 |
| A | NaN03 (NaCl) | 过量的AgN03溶液 | 溶解、过滤 |
| B | H2SO4(HCl) | 适量BaCl2溶液 | 过滤 |
| C | CO(H2O ) | 足量的浓H2SO4 | 洗气 |
| D | CuSO4 (Fe) | 足量水 | 溶解、过滤、蒸发、结晶 |
| A. | A | B. | B | C. | C | D. | D |
17.如图所示,实验现象描述错误的是( )
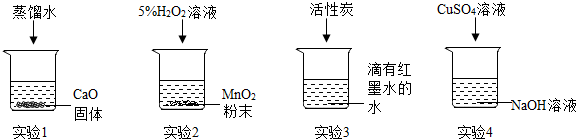

| A. | 实验1烧杯壁发烫 | B. | 实验2有气泡产生 | ||
| C. | 实验3红色逐渐变浅 | D. | 实验4无明显现象 |
14.下列有关分子、原子的说法正确的是( )
| A. | 分子在不断运动,原子不运动 | |
| B. | 吹胀气球----分子间的间隔变大 | |
| C. | 二氧化碳由碳原子和氧原子构成 | |
| D. | 电解水生成H2和O2----分子分成原子,原子重新组成新分子 |
1.实验室配制50g20%的氯化钠溶液需要经过计算、取药、称量、量取、溶解等操作.下图所对应的操作不正确的是( )
| A. | 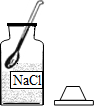 取药 | B. | 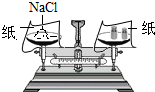 称量 称量 | ||
| C. | 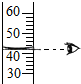 量取 | D. | 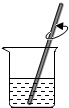 溶解 |
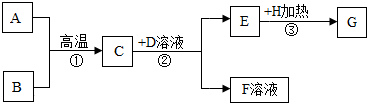
18.下列装置所示的实验中,能达到实验目的是( )
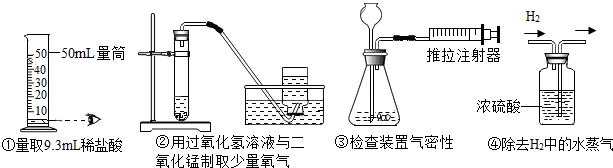

| A. | ①③ | B. | ②③ | C. | ②④ | D. | ③④ |
19.已知某两种物质在光照条件下能发生化学反应,其微观示意图如下:(说明:一种小球代表一种元素的原子)则下列说法中正确的是( )
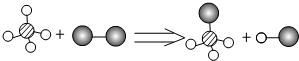
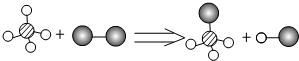
| A. | 该图示不符合质量守恒定律 | B. | 该反应属于置换反应 | ||
| C. | 图示中只有一种化合物 | D. | 该反应中分子个数比1:1:1:1 |