题目内容
5.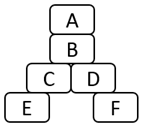 小明用六块A~F分别对应铁、二氧化碳、硫酸、氢氧化钙、碳酸钠、氯化钡的积木,搭成如图所示形状,相互接触的木块可以发生化学反应.已知D常用于中和酸性土壤,E的物质类别与其他5种不同,B与C反应可以生成F,请完成下列问题:
小明用六块A~F分别对应铁、二氧化碳、硫酸、氢氧化钙、碳酸钠、氯化钡的积木,搭成如图所示形状,相互接触的木块可以发生化学反应.已知D常用于中和酸性土壤,E的物质类别与其他5种不同,B与C反应可以生成F,请完成下列问题:(1)D的化学式为Ca(OH)2,E的名称为铁.
(2)写出A与B反应的化学方程式BaCl2+Na2CO3═BaCO3↓+2NaCl,
(3)写出C与D的反应方程式:Ca(OH)2+H2SO4═CaSO4+2H2O(基本反应类型复分解反应).
(4)写出F物质的一条用途灭火.
分析 D常用于中和酸性土壤,说明D是氢氧化钙,铁属于单质,二氧化碳、硫酸、氢氧化钙、碳酸钠、氯化钡等物质都是化合物,因此E是铁;
铁不能和二氧化碳、氢氧化钙、碳酸钠、氯化钡等物质反应,能和稀硫酸反应生成硫酸亚铁和氢气,因此C是硫酸;
碳酸钠能和硫酸反应生成硫酸钠、水和二氧化碳,能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,因此B是碳酸钠;
氯化钡能和碳酸钠反应生成碳酸钡沉淀和氯化钠,因此A是氯化钡,则F是二氧化碳.
解答 解:D常用于中和酸性土壤,说明D是氢氧化钙,铁属于单质,二氧化碳、硫酸、氢氧化钙、碳酸钠、氯化钡等物质都是化合物,因此E是铁;
铁不能和二氧化碳、氢氧化钙、碳酸钠、氯化钡等物质反应,能和稀硫酸反应生成硫酸亚铁和氢气,因此C是硫酸;
碳酸钠能和硫酸反应生成硫酸钠、水和二氧化碳,能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,因此B是碳酸钠;
氯化钡能和碳酸钠反应生成碳酸钡沉淀和氯化钠,因此A是氯化钡,则F是二氧化碳;
(1)D是氢氧化钙,氢氧化钙的化学式是Ca(OH)2;
E的名称为铁.
故填:Ca(OH)2;铁.
(2)A是氯化钡,B是碳酸钠,氯化钡和碳酸钠反应生成碳酸钡沉淀和氯化钠,反应的化学方程式为:BaCl2+Na2CO3═BaCO3↓+2NaCl.
故填:BaCl2+Na2CO3═BaCO3↓+2NaCl.
(3)C是硫酸,D是氢氧化钙,硫酸和氢氧化钙反应生成硫酸钙和水,反应的反应方程式为:Ca(OH)2+H2SO4═CaSO4+2H2O,属于复分解反应.
故填:Ca(OH)2+H2SO4═CaSO4+2H2O;复分解反应.
(4)F是二氧化碳,可以用来灭火,固体可以用作人工降雨,可以制取碳酸饮料等.
故填:灭火.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

 阅读快车系列答案
阅读快车系列答案| A. | 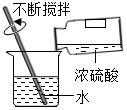 稀释浓硫酸 | B. | 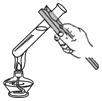 加热液体 | C. | 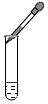 滴加少量液体 | D. | 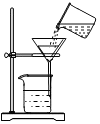 过滤 |
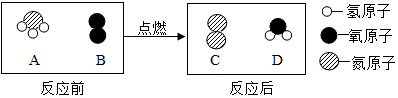
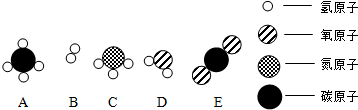
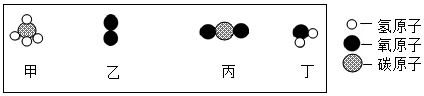
(注意:图示中没有表示物质间的微粒数量关系)
下列说法不正确的是( )
| A. | 该反应中 B 为氧化剂 | |
| B. | 生成的 C和D 的化学计量数之比为 1:1 | |
| C. | 该反应属于置换反应 | |
| D. | 该反应肯定有元素的化合价发生改变 |
| A. | 酸与碱发生中和反应时生成盐和水,因此有盐和水生成的反应一定是中和反应 | |
| B. | 碱性溶液能使石蕊试液变蓝,能使石蕊试液变蓝的溶液一定呈碱性 | |
| C. | 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 | |
| D. | 酸中都含有氢元素,所以含有氢元素的化合物一定是酸 |
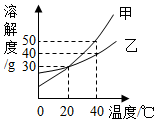 如图,是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
如图,是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )| A. | 20℃时,甲、乙两种固体物质的溶解度都是30 | |
| B. | 40℃时,甲的饱和溶液中溶质质量分数为50% | |
| C. | 40℃时,将50g乙物质全部溶于水中,恰好能得到150g乙的饱和溶液 | |
| D. | 将130g20℃甲的饱和溶液升温到40℃,最多还能溶解甲物质20g |