题目内容
1.取一定质量某Cu-Zn合金的样品与足量稀硫酸充分反应,经测定产生了0.8g气体,请计算该合金样品中锌的质量.分析 根据氢气的质量利用反应的化学方程式求出锌的质量.
解答 解:设合金中锌的质量为x
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.8g
$\frac{65}{x}=\frac{2}{0.8g}$
x=26g
答:合金样品中锌的质量分数为26g.
点评 稀硫酸是混合物,其溶质是硫酸,在做有关化学方程式的计算时,不能把稀硫酸的质量当成反应物的质量直接代入计算.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.分类法是研究和学习化学常用的一种方法.下列各组物质分类正确的是( )
| A. | 有机物:葡萄糖、一氧化碳、氨水 | |
| B. | 碱:纯碱、烧碱、熟石灰 | |
| C. | 混合物:洁净的空气、冰水共存物、生铁 | |
| D. | 合成材料:聚乙烯、涤纶、合成橡胶 |
9.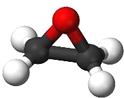 20l6年1月5日,南昌西汉海昏侯墓主棺使用泡沫材料完成套箱打包.已知制作泡沫材料的原料之一是环氧乙烷 (C2H4O),则下列关于环氧乙烷的说法正确的是( )
20l6年1月5日,南昌西汉海昏侯墓主棺使用泡沫材料完成套箱打包.已知制作泡沫材料的原料之一是环氧乙烷 (C2H4O),则下列关于环氧乙烷的说法正确的是( )
 20l6年1月5日,南昌西汉海昏侯墓主棺使用泡沫材料完成套箱打包.已知制作泡沫材料的原料之一是环氧乙烷 (C2H4O),则下列关于环氧乙烷的说法正确的是( )
20l6年1月5日,南昌西汉海昏侯墓主棺使用泡沫材料完成套箱打包.已知制作泡沫材料的原料之一是环氧乙烷 (C2H4O),则下列关于环氧乙烷的说法正确的是( )| A. | 环氧乙烷由三个元素组成 | |
| B. | 环氧乙烷分子中含有7个原子 | |
| C. | 环氧乙烷中碳元素和氢元素的质量比为1:2 | |
| D. | 环氧乙烷的相对分子质量为44,其中碳元素的质量分数最大 |
6.下列有关说法正确的是( )
| A. | 黄铜的硬度比纯铜的硬度大 | |
| B. | 可以用氢氧化钠治疗胃酸过多 | |
| C. | 地壳中含里最多的金属元素是铁 | |
| D. | 焚烧聚氯乙烯塑料不会对环境造成污染 |
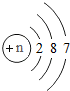 是某种元素原子结构示意图,该原子的核电荷数n为17,最外层有7个电子,在化学反应中,这种原子容易得到电子.
是某种元素原子结构示意图,该原子的核电荷数n为17,最外层有7个电子,在化学反应中,这种原子容易得到电子. 为验证质量守恒定律,某同学设计了如图实验.该实验能否达到实验目的?请说明理由.
为验证质量守恒定律,某同学设计了如图实验.该实验能否达到实验目的?请说明理由. 请你运用燃烧和灭火的相关知识,回答下列问题.
请你运用燃烧和灭火的相关知识,回答下列问题.