题目内容
12.“见著知微,见微知著”是化学思维方法.(1)从宏观知微观.
①50mL水与50mL乙醇混合后,溶液体积小于100mL,微观解释为分子间有间隔;
②气体X在氧气中燃烧生成氮气和水,X分子中一定含有的原子是N和H(填符号).
(2)从微观知宏观.
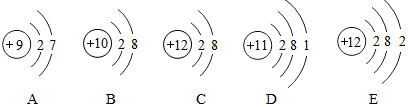
①微粒A、B的对应元素处在元素周期表中第2周期;
②微粒A、B、C、D、E中,对应单质化学性质最稳定的是B(填编号,下同),属于同一种元素的是C和E;
③微粒E对应的元素化合价是+2,微粒A、E形成的化合物的化学式为MgF2.
④甲和乙在催化剂、高温高压条件下反应生成丙,三种物质微观结构示意图如图所示,
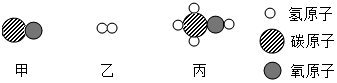
该反应的化学方程式:CO+2H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$CH3OH.
分析 (1)①根据分子间有间隔的特征分析回答;②根据质量守恒定律分析回答;
(2)①根据元素的周期数等原子的核外电子层数分析;
②根据最层电子数是8(氦为2个)的结构为稳定结构、同种元素的质子数相同分析回答;
③根据微粒的最外层电子数目的特点和元素的定义分析回答;
④根据微粒的构成分析反应物、生成物,写出反应的化学方程式.
解答 解:(1)①由于分子间有间隔,50mL水与50mL乙醇混合后,一部分乙醇分子和水分子相互占据了间隔,所以溶液体积小于100mL.
②气体X在氧气中燃烧生成氮气和水,生成物质中含有氮、氢、氧三种原子,由质量守恒定律反应前后原子的种类不变可知,X分子中一定含有的原子是N和H.
(2)①由微粒A、B的结构可知,原子的核外都有2个电子层,对应元素处在元素周期表中第2周期;
②微粒A、B、C、D、E中,B的最外层电子数是8,对应单质化学性质最稳定,C和E的质子数相同,属于同一种元素;
③微粒E的质子数12,最外层电子数是2,易失去,对应的元素化合价是+2,微粒A的质子数9,属于氟元素,化合价为-1价,A、E形成的化合物的化学式为MgF2.
④由微粒的构成的可知,该反应是一氧化碳和氢气在高温高压、催化剂条件下反应生成甲醇,反应的化学方程式为:CO+2H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$CH3OH.
故答为:(1)①分子间有间隔; ②N,H;(2)①2; ②B,C和E ③+2; MgF2;④CO+2H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$CH3OH.
点评 本题主要考查了分子的特征、原子结构示意图的意义、微粒模型图等知识,难度不大,理解图示的意义是解答本题的关键.

练习册系列答案
相关题目
3.下列解释不科学的是 ( )
| A. | 在我们的日常生活中出现了“加碘食盐”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品.这里的碘、铁、钙、硒、氟应理解为元素 | |
| B. | 严格地讲,“通风橱”是一种不负责任的防污染手段,因为实验产生的有害气体没有得到转化或吸收 | |
| C. | 长期盛放NaOH溶液的滴瓶不易打开,是因为NaOH与瓶中的CO2反应导致瓶内气体减少形成“负压”的缘故 | |
| D. | “水滴石穿”主要是溶解了CO2的雨水与CaCO3长期作用生成了可溶性的Ca(HCO3)2的缘故 |
20.地壳中含量最多的金属元素是( )
| A. | 氧 | B. | 铝 | C. | 铁 | D. | 钙 |
7.下列现象的解释中,正确的是( )
| A. | 水结冰后体积变大--水分子质量、体积非常小 | |
| B. | 金秋十月,我们在校园里能闻到桂花香味--分子不停地运动 | |
| C. | 热胀冷缩--分子大小随温度变化而改变 | |
| D. | 电解水和水蒸发变成水蒸气--前者分子本身不变,后者分子改变 |
4.下列过程中未发生化学变化的是( )
| A. |  明矾净水 | B. |  铁钉部分浸没在食盐水中 | ||
| C. |  探究燃烧的条件 | D. |  甲醛溶液浸泡动物标本 |
1.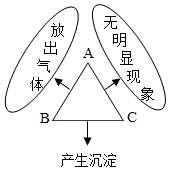 A、B、C三种溶液两两混合后的实验现象如图所示,则A、B、C三种溶液一次是( )
A、B、C三种溶液两两混合后的实验现象如图所示,则A、B、C三种溶液一次是( )
 A、B、C三种溶液两两混合后的实验现象如图所示,则A、B、C三种溶液一次是( )
A、B、C三种溶液两两混合后的实验现象如图所示,则A、B、C三种溶液一次是( )| A. | 盐酸、碳酸钠溶液、澄清石灰水 | |
| B. | 氯化钠溶液,澄清石灰水、氢氧化钠溶液 | |
| C. | 盐酸、碳酸钠溶液、氢氧化钠溶液 | |
| D. | 氢氧化钙溶液、盐酸、硫酸钠溶液 |
14.如表列出了除去物质中所含少量杂质的方法,其中错误的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CO | CO2 | 将气体缓缓通过足量的澄清石灰水,并干燥 |
| B | CO2 | CO | 将混合气体点燃 |
| C | Cu | Zn | 加入过量的稀盐酸,过滤,洗涤,烘干 |
| D | FeCl2溶液 | CuCl2 | 加入过量的铁粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |