题目内容
11.推理合理的是( )| A. | 某固体中加入稀硫酸,产生气泡,则该固体为活泼金属 | |
| B. | 某溶液中加入硫酸铜溶液,产生蓝色沉淀,则该溶液是氢氧化钠溶液 | |
| C. | 燃烧需要同时满足三个条件,则灭火也要同时控制这三个条件 | |
| D. | 某溶液进行焰色反应,火焰呈黄色,则该溶液中含有钠元素 |
分析 A、根据酸的性质解答;
B、根据硫酸铜溶液能与碱反应产生蓝色沉淀解答;
C、根据燃烧的条件和灭火的方法解答;
D、根据焰色反应解答.
解答 解:A、某固体中加入稀硫酸,产生气泡,则该固体为活泼金属或是碳酸盐,错误;
B、某溶液中加入硫酸铜溶液,产生蓝色沉淀,则该溶液是碱溶液,不一定是氢氧化钠溶液,也可以是氢氧化钙溶液,错误;
C、灭火只需要改变燃烧的其中一个条件,错误;
D、钠元素的焰色反应为黄色,正确;
故选D.
点评 本题考查的是常见的物质性质的推断,完成此题,可以依据已有的知识进行.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
2.下列实验操作正确的是( )
| A. | 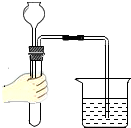 检查装置气密性 | B. | 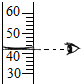 读取液体体积 | C. | 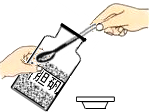 取用固体药品 | D. | 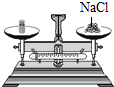 称量固体质量 |
6.既具有可燃性又具有还原性的氧化物是( )
| A. | CO | B. | CH4 | C. | H2 | D. | CO2 |
2.世界是不断变化运动的,下列变化过程中发生化学变化的是( )
| A. |  海水晒盐 | B. |  灯泡发光 | ||
| C. |  雕琢玉石 | D. |  葡萄酿酒 |