题目内容
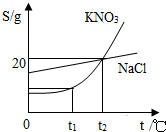 如图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( )
如图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( )| A、t1℃时,100g KNO3饱和溶液中含有20g KNO3 |
| B、NaCl 的溶解度不受温度的影响 |
| C、t2℃时,KNO3的饱和溶液和NaCl的饱和溶液中溶质的质量分数不一定相等 |
| D、温度高于t2℃时,KNO3的溶解度大于NaCl的溶解度 |
考点:固体溶解度曲线及其作用,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:A、根据溶解度概念结合题中的溶解度曲线进行分析解答;
B、根据NaCl的溶解度随温度的升高而增大,只是变化不大进行分析;
C、根据饱和时质量分数的计算公式:
×100%可知,溶解度相等则饱和溶液中溶质的质量分数一定相等进行分析;
D、根据溶解度曲线可比较同一温度下不同物质的溶解度大小进行分析.
B、根据NaCl的溶解度随温度的升高而增大,只是变化不大进行分析;
C、根据饱和时质量分数的计算公式:
| 溶解度 |
| 溶解度+100g |
D、根据溶解度曲线可比较同一温度下不同物质的溶解度大小进行分析.
解答:解:A、t1℃时,KNO3的溶解度是20g,即100gKNO3水中最多溶解20gKNO3,100gKNO3饱和溶液中含有的KNO3小于20克,故A错误;
B、NaCl的溶解度随温度的升高而增大,只是变化不大,也受温度的影响,故B错误;
C、t2℃时,氯化钠、硝酸钾的溶解度相等,所以NaCl饱和溶液与KNO3饱和溶液中溶质的质量分数一定相等,故C错误;
D、由图可知:在温度高于t2℃时,KNO3的溶解度大于NaCl的溶解度,故D正确.
故选:D.
B、NaCl的溶解度随温度的升高而增大,只是变化不大,也受温度的影响,故B错误;
C、t2℃时,氯化钠、硝酸钾的溶解度相等,所以NaCl饱和溶液与KNO3饱和溶液中溶质的质量分数一定相等,故C错误;
D、由图可知:在温度高于t2℃时,KNO3的溶解度大于NaCl的溶解度,故D正确.
故选:D.
点评:在解此类题时,首先要了解溶解度的概念、溶解度曲线的意义、溶质质量分数的计算方法,然后结合题中的选项进行分析解答.

练习册系列答案
相关题目
我国已经立法,规定酒驾入刑.“酒精检测仪”可检查司机是否酒后驾车,其反应原理为 C2H5OH+4CrO3+6H2SO4═2Cr2(SO4)3+2CO2↑+9X,司机如有饮酒,红色的CrO3就会变成绿色的Cr2(SO4)3,则X的化学式为( )
| A、Na2O |
| B、H2O |
| C、H2SO4 |
| D、CO2 |
古诗词是古人为我们留下的宝贵精神财富,下列诗句不涉及氧化还原反应的是( )
| A、野火烧不尽,春风吹又生 |
| B、春蚕到死丝方尽,蜡炬成灰泪始干 |
| C、粉身碎骨浑不怕,要留清白在人间 |
| D、爆竹声中一岁除,春风送暖入屠苏 |
下列变化不发生化学变化的是( )
A、 树木光合作用 |
B、 大理石雕像接触酸雨 |
C、 盐湖析出氯化钠 |
D、 钟乳石及石柱的形成 |
现有铁和另一种金属组成的混合物,在5.6g该混合物中加入100g一定溶质质量分数的稀盐酸,两者恰好完全反应,产生氢气的质量为m.下列说法正确的是( )
| A、若混合物为Fe、Al,m可能是0.22g |
| B、若混合物为Fe、Zn,m不可能是0.2g |
| C、若混合物为Fe、Zn,m可能是0.1g,则该混合物中铁的质量分数为50% |
| D、若混合物为Fe、A1,则稀盐酸中溶质质量分数可能大于7.3% |
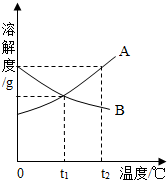 A,B两种物质的溶解度曲线如图所示
A,B两种物质的溶解度曲线如图所示