题目内容
18.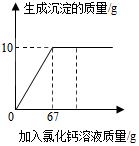 向60gNa2CO3溶液中逐滴加入一定溶质质量分数的CaCl2溶液,实验过程中生成沉淀的质量与加入CaCl2溶液的质量关系如图所示.
向60gNa2CO3溶液中逐滴加入一定溶质质量分数的CaCl2溶液,实验过程中生成沉淀的质量与加入CaCl2溶液的质量关系如图所示.(1)恰好完全反应时,生成沉淀的质量为g;
(2)计算恰好完全反应时,所得溶液中溶质的质量分数.
分析 (1)根据图中信息可以知道,恰好完全反应时,生成沉淀的质量为10g;
(2)根据(1)的分析可以知道两种溶液恰好完全反应时,所得溶液为氯化钠溶液,可以根据反应的化学方程式结合溶质的质量分数的计算公式来完成解答.
解答 解:(1)根据图中信息可以知道,恰好完全反应时,生成沉淀的质量为10g;
(2)设生成氯化钠的质量为x,
Na2CO3+CaCl2═CaCO3↓+2NaCl
100 117
10g x
$\frac{100}{10g}=\frac{117}{x}$
x=11.7g
所得溶液中溶质的质量分数:$\frac{11.7g}{60g+67g-10g}$×100%=10%
答:恰好完全反应时,所得溶液中溶质的质量分数10%.
点评 本题主要考查学生运用化学方程式和溶质的质量分数公式进行计算的能力,解答本题的关键是要分析图表的数据对应的反应.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.借助括号内的试剂,不能将组内物质鉴别出来的是( )
| A. | 固体:铁粉 氧化铜 木炭粉 (稀硫酸) | |
| B. | 固体:NaCl NaOH NH4NO3(水) | |
| C. | 溶液:NaOH Ca(OH)2 盐酸 (CO2气体) | |
| D. | 溶液:KNO3 MgCl2 盐酸 (AgNO3溶液) |
9.一定条件下,密闭容器内发生的某化学反应,测得t1和t2时各物质的质量见表,下列说法正确的是( )
| 物质 | M | N | P | Q |
| t1时的质量/g | 51 | 9 | 3 | 17 |
| t2时的质量/g | 23 | 3 | x | 51 |
| A. | x的值小于3 | B. | Q可能是单质 | ||
| C. | 该反应一定是分解反应 | D. | M与N的质量变化比为14:3 |
6.下列图示实验操作中,正确的是( )
| A. |  点燃酒精灯 | B. |  称量5.05g固体 称量5.05g固体 | ||
| C. |  加热液体 | D. |  100mL量筒量取8.5mL水 |
12.下列生产生活的材料中,不属于复合材料的是( )
| A. | 钢筋混凝土 | B. | 玻璃钢 | C. | 碳纤维复合材料 | D. | 聚乙烯塑料 |