题目内容
19.如图是某实验中各物质间的变化关系: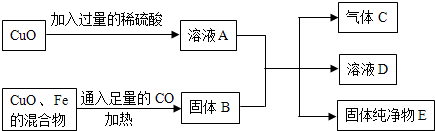
(1)写出氧化铜与稀硫酸反应的化学方程式:H2SO4+CuO═CuSO4+H2O.
(2)气体C的化学式是H2.
(3)溶液D中一定含有的溶质是FeSO4(写化学式).
分析 氧化铜和过量的硫酸反应生成硫酸铜和水,溶液A为硫酸铜和硫酸的混合溶液;一氧化碳还原氧化铜生成铜和二氧化碳,固体B中含有铁和铜;铁和硫酸生成硫酸亚铁和氢气,与硫酸铜溶液反应生成硫酸亚铁溶液和铜,故C是氢气,D中一定有硫酸亚铁,E是铜,据此进行分析解答.
解答 解:氧化铜和过量的硫酸反应生成硫酸铜和水,溶液A为硫酸铜和硫酸的混合溶液;一氧化碳还原氧化铜生成铜和二氧化碳,固体B中含有铁和铜;铁和硫酸生成硫酸亚铁和氢气,与硫酸铜溶液反应生成硫酸亚铁溶液和铜,故C是氢气,D中一定有硫酸亚铁,E是铜.
(1)氧化铜与稀硫酸反应生成硫酸铜和水,反应的化学方程式为:H2SO4+CuO═CuSO4+H2O.
(2)气体C为氢气,其化学式是H2.
(3)铁和硫酸生成硫酸亚铁和氢气,与硫酸铜溶液反应生成硫酸亚铁溶液和铜,则溶液D中一定含有的溶质是硫酸亚铁,其化学式为:FeSO4.
故答案为:(1)H2SO4+CuO═CuSO4+H2O;(2)H2;(3)FeSO4.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

练习册系列答案
相关题目
12.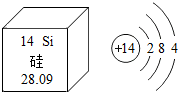 中国科技大学熊宇杰教授课题组基于应用广泛的半导体硅材料,采用金属纳米结构的热电子注入方法,设计出一种可在近红外区域进行光电转换且具有力学柔性的太阳能电池.硅的原子结构示意图及它在元素周期表的某些信息如图所示,则下列说法正确的是( )
中国科技大学熊宇杰教授课题组基于应用广泛的半导体硅材料,采用金属纳米结构的热电子注入方法,设计出一种可在近红外区域进行光电转换且具有力学柔性的太阳能电池.硅的原子结构示意图及它在元素周期表的某些信息如图所示,则下列说法正确的是( )
 中国科技大学熊宇杰教授课题组基于应用广泛的半导体硅材料,采用金属纳米结构的热电子注入方法,设计出一种可在近红外区域进行光电转换且具有力学柔性的太阳能电池.硅的原子结构示意图及它在元素周期表的某些信息如图所示,则下列说法正确的是( )
中国科技大学熊宇杰教授课题组基于应用广泛的半导体硅材料,采用金属纳米结构的热电子注入方法,设计出一种可在近红外区域进行光电转换且具有力学柔性的太阳能电池.硅的原子结构示意图及它在元素周期表的某些信息如图所示,则下列说法正确的是( )| A. | 硅是金属元素 | B. | 硅的原子序数为28 | ||
| C. | 硅的相对原子质量为14 | D. | 硅的最外层电子数为4 |
10.将10%的氨水与20%的氨水等体积混合时溶质质量分数( )
| A. | 15% | B. | >15% | C. | <15% | D. | 上述情况均可能 |
8.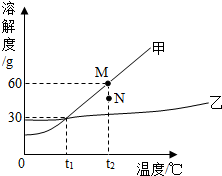 如图为甲﹑乙两物质的溶解度曲线.下列说法不正确的是( )
如图为甲﹑乙两物质的溶解度曲线.下列说法不正确的是( )
 如图为甲﹑乙两物质的溶解度曲线.下列说法不正确的是( )
如图为甲﹑乙两物质的溶解度曲线.下列说法不正确的是( )| A. | 甲的溶解度受温度变化影响比乙大 | |
| B. | t1℃时,甲、乙两物质饱和溶液中溶质的质量分数相同 | |
| C. | 要使组成在N点的甲溶液转变为M点的甲溶液,可以采用升高温度的方法 | |
| D. | 乙采用蒸发溶剂的方法得到乙晶体 |
9.从水分子分解示意图中我们能获得许多信息,其中描述错误的是( )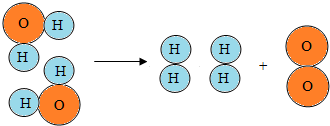

| A. | 该反应过程中元素的种类不变 | B. | 该反应过程中分子的种类不变 | ||
| C. | 在化学变化中原子是最小的粒子 | D. | 氢分子能保持氢气的化学性质 |
