题目内容
8.实验一:粗盐提纯的部分操作如图1所示.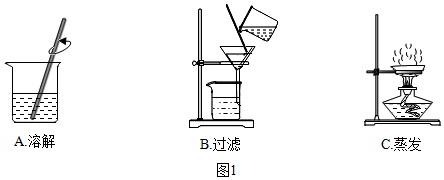
(1)操作A中使用玻璃棒搅拌的作用是加速溶解.
(2)制作过滤器的过程如图2所示,其正确操作顺序为③①②(填序号).

(3)操作B结束后发现滤液仍较浑浊,可能的原因是滤纸破裂(写一点).
(4)举出一个生活中应用过滤原理的实例:自来水厂的过滤池.
实验二:中和反应是放热反应吗?三位同学为探究此问题进行了下列实验:

(1)甲同学取10mL 10%的NaOH溶液于试管中,逐滴加入10%的稀硫酸,随着硫酸的加入,烧杯中溶液温度与加入硫酸体积之间的变化关系如图3甲所示.本实验选用10%的NaOH溶液而不选用NaOH固体的原因是氢氧化钠固体溶于水放热.
(2)乙同学按图3乙装置进行实验,其中的澄清饱和石灰水的作用是通过饱和石灰水变浑浊证明反应放热.
(3)丙同学按图3丙实验,可以根据烧杯中的导管口产生气泡的现象也能证明中和反应是放热的.
分析 实验一:玻璃棒用途有搅拌、引流、转移物质等;
制作过滤器的过程如图2所示,其正确操作顺序为③①②;
过滤时,如果滤纸破裂、液面高于滤纸边缘,都能够导致滤液浑浊;
自来水厂的过滤池在净化水的过程中起到过滤的作用;
实验二:氢氧化钠固体溶于水放热;
氢氧化钙的溶解度随着温度升高而减小;
气体的压强随着温度升高而增大.
解答 解:实验一:(1)操作A中使用玻璃棒搅拌的作用是加速溶解.
故填:加速溶解.
(2)制作过滤器的过程如图2所示,其正确操作顺序为③①②.
故填:③①②.
(3)操作B结束后发现滤液仍较浑浊,可能的原因是滤纸破裂,液面高于滤纸边缘等.
故填:滤纸破裂.
(4)生活中自来水厂的过滤池在净化水的过程中起到过滤的作用.
故填:自来水厂的过滤池.
实验二:(1)本实验选用10%的NaOH溶液而不选用NaOH固体的原因是氢氧化钠固体溶于水放热,影响对反应是否放热的判断.
故填:氢氧化钠固体溶于水放热.
(2)氢氧化钙的溶解度随着温度升高而减小,通过观察石灰水变浑浊可以判断中和反应是放热的.
故填:通过饱和石灰水变浑浊证明反应放热.
(3)如果中和反应是放热的,会导致瓶中气体压强增大,从而导致部分气体从烧杯中的导管口逸出,逸出可以根据烧杯中的导管口产生气泡能证明中和反应是放热的.
故填:烧杯中的导管口产生气泡.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.首饰店中的项链上标有18K,其含金量为( )
| A. | 25% | B. | 75% | C. | 45% | D. | 85% |
19.下列物质的俗名、化学名称和化学式相一致的是( )
| A. | 生石灰、氧化钙、CaO | B. | 纯碱、氢氧化钠、NaOH | ||
| C. | 石灰石、氢氧化钙、Ca(OH)2 | D. | 熟石灰、碳酸钙、CaCO3 |
17.我们生活在物质的世界里,而物质在不断地变化.下列四个变化中,与其他三个变化有本质区别的是( )
| A. | 铁生锈 | B. | 蜡烛燃烧 | C. | 加热高锰酸钾 | D. | 工业制取氧气 |
18.某化学兴趣小组的同学按照课本的实验装置做“测定空气中氧气的体积分数”实验(图1),但测出的氧气体积分数明显小于$\frac{1}{5}$.请你参与探究:
【提出问题】造成误差的原因是什么?如何改进课本实验装置?
【查阅资料】(1)着火点是指可燃物燃烧所需要的最低温度.
(2)白磷和红磷的组成元素、燃烧现象和产物均相同.
(3)铜在空气中加热,和氧气反应生成黑色的氧化铜.

【猜想与假设】
甲同学:可能是导管内原存有空气,后来留有吸入的水,影响实验的准确性;
乙同学:可能是瓶内残留气体中还有氧气的缘故;
你还能做的猜想是红磷不足等
【交流与讨论】
(1)丙同学认为,用木炭代替红磷,就可以消除这个现象,大家认为丙同学的猜想不合理,理由是木炭可以和氧气反应生成二氧化碳气体,不能产生压强差;
(2)他们对课本实验装置进行了如图2的改进(其他仪器忽略).
①甲同学提出应把红磷更换为白磷,理由是白磷的着火点低,可以较容易的发生燃烧,
白磷燃烧的符号表达式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
②通过粗铜丝来点燃玻璃管内的白磷,利用了金属铜的物理性质是导电性;
③与课本实验装置相比,该装置的一个优点是环保,生成的五氧化二磷有毒,不污染空气;测量所得数据比较准确;所用试剂量少,节约药品等.
【探究与反思】
(1)为验证乙同学的猜想,将铜粉在残余气体中加热,观察到铜粉变黑,所以乙同学的猜想合理(选填“合理”或“不合理”).
(2)大家采用改进的实验装置(图2)进行实验,待玻璃管冷却、管内白色的烟幕消失,左管液面上升了1格,得到了较准确的数据,但又意外发现左玻璃管内壁上端附着黄色固体.黄色固体主要成分可能是白磷.
【提出问题】造成误差的原因是什么?如何改进课本实验装置?
【查阅资料】(1)着火点是指可燃物燃烧所需要的最低温度.
(2)白磷和红磷的组成元素、燃烧现象和产物均相同.
(3)铜在空气中加热,和氧气反应生成黑色的氧化铜.
| 颜色、状态 | 熔点/℃ | 着火点/℃ | 密度/g•cm-3 | |
| 红磷 | 暗红色固体 | 590 | 240 | 2.34 |
| 白磷 | 白色或黄色固体 | 44.1 | 40 | 1.82 |

【猜想与假设】
甲同学:可能是导管内原存有空气,后来留有吸入的水,影响实验的准确性;
乙同学:可能是瓶内残留气体中还有氧气的缘故;
你还能做的猜想是红磷不足等
【交流与讨论】
(1)丙同学认为,用木炭代替红磷,就可以消除这个现象,大家认为丙同学的猜想不合理,理由是木炭可以和氧气反应生成二氧化碳气体,不能产生压强差;
(2)他们对课本实验装置进行了如图2的改进(其他仪器忽略).
①甲同学提出应把红磷更换为白磷,理由是白磷的着火点低,可以较容易的发生燃烧,
白磷燃烧的符号表达式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
②通过粗铜丝来点燃玻璃管内的白磷,利用了金属铜的物理性质是导电性;
③与课本实验装置相比,该装置的一个优点是环保,生成的五氧化二磷有毒,不污染空气;测量所得数据比较准确;所用试剂量少,节约药品等.
【探究与反思】
(1)为验证乙同学的猜想,将铜粉在残余气体中加热,观察到铜粉变黑,所以乙同学的猜想合理(选填“合理”或“不合理”).
(2)大家采用改进的实验装置(图2)进行实验,待玻璃管冷却、管内白色的烟幕消失,左管液面上升了1格,得到了较准确的数据,但又意外发现左玻璃管内壁上端附着黄色固体.黄色固体主要成分可能是白磷.