题目内容
4.单质硅是制作电子集成电路的基础材料,工业上通过以下反应将自然界中的二氧化硅(SiO2)转化为硅(Si):SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,下列分析正确的是( )| A. | 二氧化硅发生了氧化反应 | B. | 碳发生了还原反应 | ||
| C. | 碳表现出了还原性 | D. | 该反应属于分解反应 |
分析 根据题意,自然界中的二氧化硅(SiO2)转化为硅(Si)的反应为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,该反应中二氧化硅失去了氧,碳夺取了二氧化硅中的氧,据此结合题意进行分析判断.
解答 解:自然界中的二氧化硅(SiO2)转化为硅(Si)的反应为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
A、该反应中二氧化硅失去了氧,发生了还原反应,故选项说法错误.
B、该反应中碳夺取了二氧化硅中的氧,发生了氧化反应,故选项说法错误.
C、该反应中碳夺取了二氧化硅中的氧,发生了氧化反应,具有还原性,故选项说法正确.
D、该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项说法错误.
故选:C.
点评 本题难度不大,掌握碳的化学性质、氧化反应、还原反应、置换反应的特征等是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.下列典故主要体现化学变化的是( )
| A. | 火烧赤壁 | B. | 铁杵磨成针 | C. | 司马光砸缸 | D. | 凿壁偷光 |
19.下列微粒的示意图中,表示阳离子的是( )
| A. | 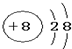 | B. | 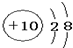 | C. | 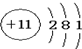 | D. | 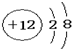 |
9. 氯化钾和硝酸钾晶体在不同温度时的溶解度如下表所示.
氯化钾和硝酸钾晶体在不同温度时的溶解度如下表所示.
(1)若两物质的溶解度相等,此时所对应的温度范围在20℃~30℃之间.
(2)在20℃时,将35gKCl加入到100g水中,形成的KCl溶液的质量为134g,将温度升到40℃,形成的溶液不饱和 (选填“饱和”或“不饱和”)溶液.
(3)图中能表示KCl溶解度曲线的是b (选填“a”或“b”).
 氯化钾和硝酸钾晶体在不同温度时的溶解度如下表所示.
氯化钾和硝酸钾晶体在不同温度时的溶解度如下表所示.| 0 | 10 | 20 | 30 | 40 | |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 |
(2)在20℃时,将35gKCl加入到100g水中,形成的KCl溶液的质量为134g,将温度升到40℃,形成的溶液不饱和 (选填“饱和”或“不饱和”)溶液.
(3)图中能表示KCl溶解度曲线的是b (选填“a”或“b”).
16.(1)如图是某实验小组的同足额绘制的两种固体物质的溶解度曲线图.请你根据图示回答问题:

①t1℃时,a物质的溶解度<b 物质的溶解度(填“>”、“<”或“=”).
②将t2℃时相同质量的a、b两种物质的饱和溶液,分别冷却到t1℃,析出晶体最多的是a物质.
③溶解度曲线图中的任何一点都表示溶液的一种特定状态.图中A、B两个状态中,溶液属于不饱和状态的是B.
④t1℃时,将等质量的a、b两种物质加水溶解配制成饱和溶液,所得溶液质量的大小关系为:a>b(填“>”、“<”或“=”).
(2)海洋资源十分丰富.从海水中提取氯化钠并以氯化钠和水为原料制取氢氧化钠、氯气等物质的工艺流程图如图:

某兴趣小组进行如下实验:
【实验一】除去粗盐中的不溶性杂质
步骤一:用托盘天平称取5.0g粗盐,用药匙,用药匙将该粗盐逐渐加入盛10.0ml水的烧杯里,边加边用玻璃棒搅拌,已知加到粗盐不再溶解为止.称量剩下的粗盐质量为1.4g.
步骤二:经过滤、蒸发,得到3.2g精盐.
①计算精盐的产率88.9%(精确到0.1%).
②步骤I、II的部分操作如图所示,其中错误的是Ⅱ(填标号).

【实验二】探究工艺流程图步骤Ⅱ所得的氯化钠溶液中MgCl2是否除尽,溶液中是否含有CaCl2
[查阅资料]有关物质的溶解性表(20℃)
[进行实验]请你与他们共同完成,并回答所给的问题:
【拓展思维】
①工艺流程图步骤Ⅰ从海水中得到粗盐,采用风吹日晒蒸发溶剂的方法,而不是采用降低溶液温度的方法,原因是氯化钠的溶解度受温度影响较小.
②写出工艺流程图步骤Ⅳ的化学方程式2NaCl+H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑.

①t1℃时,a物质的溶解度<b 物质的溶解度(填“>”、“<”或“=”).
②将t2℃时相同质量的a、b两种物质的饱和溶液,分别冷却到t1℃,析出晶体最多的是a物质.
③溶解度曲线图中的任何一点都表示溶液的一种特定状态.图中A、B两个状态中,溶液属于不饱和状态的是B.
④t1℃时,将等质量的a、b两种物质加水溶解配制成饱和溶液,所得溶液质量的大小关系为:a>b(填“>”、“<”或“=”).
(2)海洋资源十分丰富.从海水中提取氯化钠并以氯化钠和水为原料制取氢氧化钠、氯气等物质的工艺流程图如图:

某兴趣小组进行如下实验:
【实验一】除去粗盐中的不溶性杂质
步骤一:用托盘天平称取5.0g粗盐,用药匙,用药匙将该粗盐逐渐加入盛10.0ml水的烧杯里,边加边用玻璃棒搅拌,已知加到粗盐不再溶解为止.称量剩下的粗盐质量为1.4g.
步骤二:经过滤、蒸发,得到3.2g精盐.
①计算精盐的产率88.9%(精确到0.1%).
②步骤I、II的部分操作如图所示,其中错误的是Ⅱ(填标号).

【实验二】探究工艺流程图步骤Ⅱ所得的氯化钠溶液中MgCl2是否除尽,溶液中是否含有CaCl2
[查阅资料]有关物质的溶解性表(20℃)
| 阴离子 阳离子 | OH- | CO32- |
| Ca2+ | 微 | 不 |
| Mg2+ | 不 | 微 |
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤一:取一定量的氯化钠溶液于试管中,加入适量的NaOH溶液 | 无明显现象 | 说明MgCl2已(填“已”或“未”)除尽 |
| 步骤二:往步骤一所得溶液中加入适量的Na2CO3 溶液 | 产生白色沉淀 | 说明溶液中含有CaCl2 |
①工艺流程图步骤Ⅰ从海水中得到粗盐,采用风吹日晒蒸发溶剂的方法,而不是采用降低溶液温度的方法,原因是氯化钠的溶解度受温度影响较小.
②写出工艺流程图步骤Ⅳ的化学方程式2NaCl+H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑.
13.如图为制取水煤气(混合气体)的微观示意图,下列说法中正确的是( )

| A. | 该反应中含两种有机化合物 | B. | 水煤气的成分是一氧化碳和氧气 | ||
| C. | 该反应为置换反应 | D. | 该反应中反应物的质量比为8:9 |
14.小马的午餐是:红烧牛肉、米饭、豆腐汤,从均衡营养角度建议增加( )
| A. | 炒鸡蛋 | B. | 牛奶 | C. | 炒油菜 | D. | 烤鸭 |