题目内容
日常生活中加碘食盐、高钙牛奶中的“碘”和“钙”指的是( )
A. 单质 B. 分子 C. 原子 D. 元素
如表是某同学错题本中整理的部分内容,其中不需要修改的是
A.化学用语 | B.仪器使用 |
氧化铝―AlO 2Ca2+―表示两个钙离子 | 直接在酒精灯火焰上加热的玻璃仪器―试管 胶头滴管取用试剂后―倒置或平放 |
C.物质的性质与用途 | D.物质鉴别 |
氦气密度小―填充探空气球 氮气常温下化学性质稳定―制氮肥、炸药 | 二氧化碳、氧气―加澄清石灰水 过氧化氢溶液、水―加二氧化锰 |
A. A B. B C. C D. D
某化学课堂围绕“酸碱中和反应”进行探宄活动.
(演示实验)将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式是______。
(查阋资料)CaC12溶液显中性
(提出问题)实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
(猜想与假设)针对疑问,甲组同学猜想如下:
猜想a:只有CaC12
猜想b:有_______(填化学式)
猜想c:有CaC12和Ca(OH)2
(实验探究)为了验证猜想,乙小组进行了下列三个方案的探究。
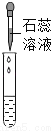
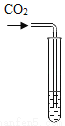
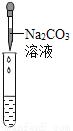
实验方案 | 滴加紫色石蕊试液 | 通入CO2 | 滴加Na2CO3溶液 |
实验操作 |
|
|
|
实验现象 | 石蕊试液变蓝 | _________ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
(得出结论)通过探究,同学们一致确定猜想_________(填写字母)是正确的。
(评价反思)(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因_______________。
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外.还需要考虑____________。
下列实验所对应的两种方案均正确的是
选项 | 目的 | 方案一 | 方案二 |
A | 除去二氧化碳中的少量水蒸气 | 通过浓硫酸 | 通过碱石灰 |
B | 检验NaOH是否变质 | 加足量稀盐酸,观察 | 加适量氯化钡溶液,观察 |
C | 将CuSO4转化成FeSO4 | 加过量的铁,反应后过滤 | 加氢氧化铁,反应后过滤 |
D | 鉴别化肥NH4C1和NH4NO3 | 取样,加水溶解,观察 | 取样,加熟石灰研磨 |
A. A B. B C. C D. D