题目内容
将某赤铁矿石样品10g放入盛有适量稀盐酸的烧杯中,恰好完全反应,反应后烧杯中物质的总质量
为114.5g,过滤后将固体洗涤、干燥,称其质量为2g.(杂质不溶于水也不反应)求:
(1)赤铁矿石样品中氧化铁的质量分数
(2)稀盐酸的溶质质量分数.
为114.5g,过滤后将固体洗涤、干燥,称其质量为2g.(杂质不溶于水也不反应)求:
(1)赤铁矿石样品中氧化铁的质量分数
(2)稀盐酸的溶质质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)固体剩余的质量是杂质的质量,由杂质的质量可计算出赤铁矿石中氧化铁的质量,由氧化铁的质量可计算出赤铁矿石中氧化铁的质量分数;
(2)由氧化铁和稀盐酸恰好完全反应,由氧化铁的质量可以根据化学方程式计算出消耗氯化氢的质量,进而计算出稀盐酸的溶质质量分数.
(2)由氧化铁和稀盐酸恰好完全反应,由氧化铁的质量可以根据化学方程式计算出消耗氯化氢的质量,进而计算出稀盐酸的溶质质量分数.
解答:解:
(1)赤铁矿石样品中氧化铁的质量分数
×100%=80%;
(2)设,稀盐酸的溶质质量为x,
Fe2O3+6HCl=2FeCl3+3H2O
160 219
10g-2g x
=
x=10.95g,
稀盐酸的溶质质量分数:
×100%=10%
答:(1)赤铁矿石样品中氧化铁的质量分数是80%;
(2)稀盐酸的溶质质量分数是10%.
(1)赤铁矿石样品中氧化铁的质量分数
| 10g-2g |
| 10g |
(2)设,稀盐酸的溶质质量为x,
Fe2O3+6HCl=2FeCl3+3H2O
160 219
10g-2g x
| 160 |
| 10g-2g |
| 219 |
| x |
x=10.95g,
稀盐酸的溶质质量分数:
| 10.95g |
| 114.5g-10g |
答:(1)赤铁矿石样品中氧化铁的质量分数是80%;
(2)稀盐酸的溶质质量分数是10%.
点评:掌握化学方程式的计算格式和规范性,学会分析题意从中得到一些解题的信息和方法.

练习册系列答案
相关题目
分类是化学学习、研究的重要方法.下列有关物质的分类错误的是( )
| A、水属于氧化物 |
| B、干冰属于单质 |
| C、硝酸铵属于盐 |
| D、乙醇属于有机物 |
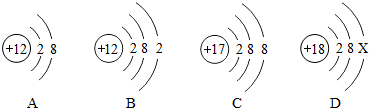
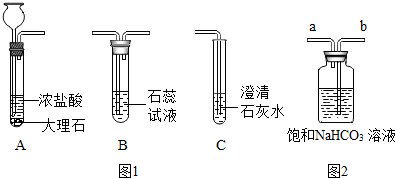 小明用如图1装置制取气体并验证气体的性质,请回答:
小明用如图1装置制取气体并验证气体的性质,请回答:
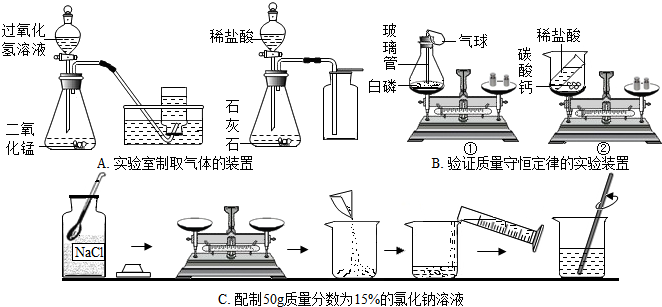
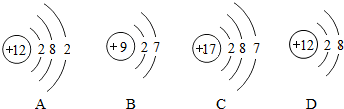
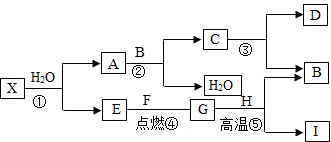 钙的过氧化物X是一种安全无毒的物质,常用作长途运输时鱼苗的供氧剂.已知X含有的两种元素的质量比为5:4.由X出发有下列转化关系,其中⑤是工业中冶炼目前使用最广泛的一种金属I 的反应,B、E、G是常见的气体,E、F是非金属单质,B能使澄清石灰水变浑浊.回答下列问题:
钙的过氧化物X是一种安全无毒的物质,常用作长途运输时鱼苗的供氧剂.已知X含有的两种元素的质量比为5:4.由X出发有下列转化关系,其中⑤是工业中冶炼目前使用最广泛的一种金属I 的反应,B、E、G是常见的气体,E、F是非金属单质,B能使澄清石灰水变浑浊.回答下列问题: 如表8种物质为初中常见物质,均由表中元素组成.
如表8种物质为初中常见物质,均由表中元素组成.