题目内容
19.有20g氢氧化鎂和氧化铁组成的固体混合物,为了测定此混合物中氧元素的质量分数,将此混合物倒入烧杯中,并取100g溶质质量分数为14.6%的稀盐酸加入烧杯中,充分反应后,烧杯中只得到黄色中性溶液(题中涉及的盐溶液均认为中性),黄色溶液中溶剂质量为94.4g.则原固体混合物中氧元素的质量分数为40%.分析 氢氧化镁和稀盐酸反应生成氯化镁和水,氧化铁和稀盐酸反应生成氯化铁和水,黄色溶液中溶剂质量为94.4g,包括稀盐酸中的水和反应生成的水,反应生成的水中的氧元素质量即为氢氧化镁和氧化铁中氧元素的质量.
解答 解:100g溶质质量分数为14.6%的稀盐酸中水的质量为:100g-100g×14.6%=85.4g,
反应生成水的质量为:94.4g-85.4g=9g,
即氢氧化镁和氧化铁中氧元素的质量为:9g×$\frac{16}{18}$×100%=8g,
则原固体混合物中氧元素的质量分数为:$\frac{8g}{20g}$×100%=40%,
故填:40%.
点评 本题是借助于数学模型,利用公式来分析和解决化学计算中的有关问题,要求学生有较强的数据分析能力.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
10.如图所示图示的实验中,正确的是( )
| A. |  将NaCI倒入量筒中配制溶液 | B. | 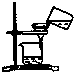 过滤 | ||
| C. | 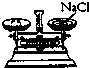 称取NaCI | D. | 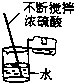 稀释浓硫酸 |
7.下列区分物质的方法中,错误的是( )
| A. | 硬水和软水:用肥皂水,观察产生泡沫的多少 | |
| B. | 石灰水与氢氧化钠溶液:滴加酚酞溶液,观察颜色是否改变 | |
| C. | 氧气与二氧化碳:用燃着的木条,观察木条是否熄灭 | |
| D. | 鉴别稀盐酸和稀硫酸:分别取样,滴加少量Ba(NO3)2溶液 |
14.某密闭容器中含有甲、乙、丙、丁四种物质,在一定条件下充分反应后,测得有关数据如下表.下列说法错误的是( )
| 物 质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 1.7 | 1.3 | 5 | 7 |
| 反应后质量/g | 待测 | 12.3 | 1 | 0 |
| A. | 待测的值是1.7 | B. | 丙、丁在反应中的质量比为4:7 | ||
| C. | 物质甲可能是催化剂 | D. | 物质乙属于单质 |
4.下列物质的用途与性质不相对应的是( )
| A. |  氢气密度小 | B. |  氧气能供给呼吸 | ||
| C. |  干冰升华吸收大量的热 | D. |  合金高强度、耐高温 |
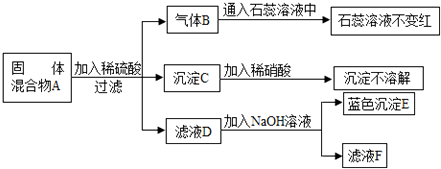
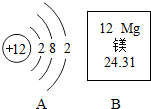 图A为镁原子的结构示意图,图B是镁元素在元素周期表中的部分信息,据此回答下列问题.
图A为镁原子的结构示意图,图B是镁元素在元素周期表中的部分信息,据此回答下列问题.