题目内容
黄铜是铜、锌合金,它可用来制造机器、电器零件及日用品。为测定某黄铜样品中铜的质量分数,现取10 g该样品粉碎,加入到50 g稀硫酸中,恰好完全反应,测得剩余固体质量为3.5 g。计算:
(1)黄铜样品中铜的质量分数。
(2)稀硫酸中溶质的质量分数。
(3)由此得到启示是:在使用黄铜制品时应注意
。(合理即可)
(1)黄铜样品中铜的质量分数为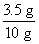 ×100%=35%
×100%=35%
(2)10 g该样品中,锌的质量为10 g-3.5 g=6.5 g
设稀硫酸中溶质的质量为x
Zn + H2SO4====ZnSO4+H2↑
65 98
6.5 g x
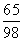 =
=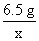
x=9.8 g
稀硫酸中溶质的质量分数为
 ×100%=19.6%
×100%=19.6%
答案:(1)黄铜样品中铜的质量分数为35%。
(2)稀硫酸中溶质的质量分数为19.6%。
(3)避免与酸接触(合理即可)

练习册系列答案
相关题目
下列操作或现象与分子对应的特性不一致的选项是
| 选项 | 操作或现象 | 分子的特性 |
| A | 给篮球充气 | 分子间有间隔 |
| B | 100mL酒精和100mL水混合在一起,体积小于200mL | 分子是有质量的 |
| C | 在花园中可闻到花的香味 | 分子是不断运动的 |
| D | 水通电分解可得到氢气和氧气 | 化学变化中分子是可以再分的 |




