题目内容
16.由(NH4)2S、(NH4)2SO4、(NH4)2HPO4组成的混合物中,已知氮元素的质量分数是28%,则混合物中氧元素的质量分数为( )| A. | 16% | B. | 32% | C. | 64% | D. | 无法确定 |
分析 观察三种化合物的结构,不难发现只有最后一种存在磷元素,三种化合物中相对原子质量存在一定的比例关系,即:(NH4)2S中(NH4)2S和N的关系是68:28、(NH4)2SO4中也是、(NH4)2HPO4中(NH4)2HP和N的关系是68:28,所以已知氮元素的质量分数,可以求出(NH4)2S或(NH4)2HP的质量分数,进一步可求出氧元素的质量分数.
解答 解:已知氮元素的质量分数为28%,
则(NH4)2S或(NH4)2HP的质量分数=$\frac{68}{28}$×28%=68%,
氧元素的质量分数为:1-68%=32%.
故选B.
点评 此题考查混合物中某元素的质量计算,需要仔细观察所给物质的化学式,从中找出元素组成规律,才能正确解答.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
6.空气是人类生存所必需的重要资源.下列物质发生的变化与空气成分无关的是( )
| A. | 木柴燃烧 | B. | 酥脆的饼干在空气中逐渐变软 | ||
| C. | 光合作用 | D. | 糖溶于水后水变甜 |
4.已知氰化钠中氮元素的化合价为-3价,则碳元素的化合价为( )
| A. | +4 | B. | +2 | C. | -4 | D. | -2 |
8.小红观察了在不同酸碱度下紫甘蓝汁液所显示的颜色,记录如图:
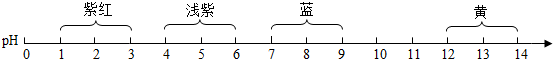
下列物质中,能使紫甘蓝汁液变黄的是( )

下列物质中,能使紫甘蓝汁液变黄的是( )
| A. | 食醋 | B. | 食盐溶液 | C. | 苏打溶液 | D. | 水 |
5.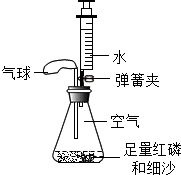 实验小组用如图装置测定空气中的氧气含量,锥形瓶中空气的体积为100mL,注射器中水的体积为25mL,装置气密性良好.下列说法不正确的是( )
实验小组用如图装置测定空气中的氧气含量,锥形瓶中空气的体积为100mL,注射器中水的体积为25mL,装置气密性良好.下列说法不正确的是( )
 实验小组用如图装置测定空气中的氧气含量,锥形瓶中空气的体积为100mL,注射器中水的体积为25mL,装置气密性良好.下列说法不正确的是( )
实验小组用如图装置测定空气中的氧气含量,锥形瓶中空气的体积为100mL,注射器中水的体积为25mL,装置气密性良好.下列说法不正确的是( )| A. | 气球的作用是缓冲装置中的压强变化 | |
| B. | 瓶底的细沙可以防止红磷燃烧时集气瓶炸裂 | |
| C. | 红磷熄灭后应该等装置冷却到室温,再打开弹簧夹观察现象 | |
| D. | 打开弹簧夹后,注射器中的水一定全部进入锥形瓶中 |
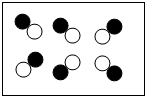

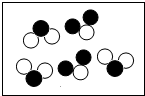

 某化学兴趣小组利用右下图所示装置来研究微粒的性质,过程如下:
某化学兴趣小组利用右下图所示装置来研究微粒的性质,过程如下: