题目内容
13.在化学课上,甲同学将燃烧的钠迅速伸入到盛有CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上黏附着白色物质.【提出问题】黑色颗粒和白色物质是什么?
【进行猜想】甲认为黑色颗粒是碳,白色物质可能是Na2O或Na2CO3,乙同学还认为白色物质是氢氧化钠.甲同学立刻认为乙同学的猜想是错误的,其理由是反应物中不含有氢元素,因此不能生成氢氧化钠
【查阅资料】氧化钠为白色粉末,溶于水生成氢氧化钠:Na2O+H2O═2NaOH
【实验探究】甲同学对白色物质进行实验探究.
| 实验方案 | 实验操作 | 实验 现象 | 结论 |
| 方案1 | 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
| 方案2 | ①取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 | 白色物质是Na2CO3. |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
【得出结论】钠在二氧化碳中燃烧的化学方程式为4Na+3CO2$\frac{\underline{\;点燃\;}}{\;}$2Na2CO3+C.
分析 【进行猜想】
化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变;
【实验探究】
氢氧化钠溶液、碳酸钠溶液都是显碱性的溶液,都能够使酚酞试液变红色;
碳酸钠能和氯化钙反应生成白色沉淀碳酸钙和氯化钠;
【得出结论】
钠在二氧化碳中燃烧生成碳酸钠和碳.
解答 解:【进行猜想】
碳是黑色固体,因此甲认为黑色颗粒是碳,白色物质可能是Na2O或Na2CO3;
甲同学认为乙同学的猜想是错误的,其理由是反应物中不含有氢元素,因此不能生成氢氧化钠.
故填:碳;Na2CO3;反应物中不含有氢元素,因此不能生成氢氧化钠.
【实验探究】
实验过程如下表所示:
| 实验方案 | 实验操作 | 实验 现象 | 结论 |
| 方案1 | 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
| 方案2 | ①取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 | 白色物质是Na2CO3. |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
丙同学认为方案1得到的结论不正确,其理由是碳酸钠溶液显碱性,也能使酚酞试液变红色.
故填:碳酸钠溶液显碱性,也能使酚酞试液变红色.
【得出结论】
钠在二氧化碳中燃烧生成碳酸钠和碳,反应的化学方程式为:4Na+3CO2$\frac{\underline{\;点燃\;}}{\;}$2Na2CO3+C.
故填:4Na+3CO2$\frac{\underline{\;点燃\;}}{\;}$2Na2CO3+C.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
10.物质的用途与性质密切相关.下列叙述错误的是( )
| A. | 因为熟石灰能和酸发生反应,所以可用熟石灰改良酸性土壤 | |
| B. | 因为“洗洁精”有乳化功能,所以“洗洁精”可用来洗涤餐具上的油污 | |
| C. | 因为CO易溶于水,故在室内放一盆水能预防煤气中毒 | |
| D. | 因为氮气化学性质不活泼,所以可用于食品包装袋内防腐 |
4.可用于鉴别HCl溶液和NaOH溶液的试剂或方法是( )
| A. | 观察颜色 | B. | NaCl溶液 | C. | 酚酞溶液 | D. | Ca(OH)2溶液 |
1.化学对社会发展的重要贡献之一,就是不断研发新型材料,玻璃属于( )
| A. | 非金属材料 | B. | 有机合成材料 | C. | 金属材料 | D. | 复合材料 |
8.某化工厂的废液中含有硝酸银、硝酸铜和硝酸锌.某同学取适量的上述废液样品,将一定质量的铝粉加入样品中,充分反应后过滤,得到无色滤液和滤渣.下列判断正确的是( )
| A. | 滤出的固体中一定含有银,可能含有铜、锌 | |
| B. | 滤出的固体中一定含有银和铜,可能含有锌 | |
| C. | 滤液中一定含有硝酸铝、硝酸锌,一定没有硝酸铜和硝酸银 | |
| D. | 加入铝粉反应后得到滤液的质量大于反应前滤液的质量 |
5.下列说法正确的是( )
| A. | 油脂.糖类、蛋白质都是人体必需的营养素,撬入得越多越好 | |
| B. | 为防止水污染,应禁止使用化肥和农药 | |
| C. | 吃水果和蔬菜可以补充维生素 | |
| D. | 用洗洁精去油污是因为洗洁精能溶解油污 |
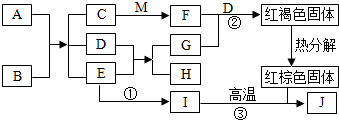 D、E、I都属于氧化物,A是人体胃液的主要成分之一,C为浅绿色溶液,E常用作温室肥料,G是空气中的主要成分之一,H为有机物,J是常见金属,M是一种常见的碱.它们的转化关系如右图,部分物质略去.
D、E、I都属于氧化物,A是人体胃液的主要成分之一,C为浅绿色溶液,E常用作温室肥料,G是空气中的主要成分之一,H为有机物,J是常见金属,M是一种常见的碱.它们的转化关系如右图,部分物质略去.