题目内容
8.自来水消毒过程中会发生以下变化,其微观过程可用如图表示: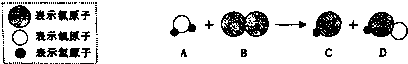
(1)该变化属于化学变化(填“物理”或“化学”),理由是变化成了新分子.
(2)A物质属于化合物.(填“化合物”或“单质”)
(3)分析以上微观过程模拟图,你能总结出的一条结论是化学变化中原子的种类和个数不发生改变.
分析 观察微观过程图,根据微粒的变化分析变化的类型、分析分子、原子的变化等,根据微粒的构成分析物质的类别等.
解答 解:(1)该变化属于化学变化,理由是变化成了新分子.
(2)A物质的分子是由不同种原子构成的,属于化合物.
(3)分析以上微观过程模拟图,由微粒的变化可知:化学变化中原子的种类和个数不发生改变.
故答为:(1)化学,变化生成了新分子;(2)化合物;(3)化学变化中原子的种类和个数不发生改变.
点评 解答本题要充分理解图中提供的信息,只有这样才能确定物质的构成及种类,也才能正确的判断物质的化学式、反应的方程式和反应类型等.

练习册系列答案
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
19.下列两种物质混合后,能发生化学反应且溶液质量增加的是( )
| A. | 氢氧化钠溶液和稀盐酸 | B. | 铜和硝酸银溶液 | ||
| C. | 氧化铜固体和稀盐酸 | D. | 碳酸钠溶液和氢氧化钙溶液 |
16. 如表是KNO3、NaCl在不同温度下的部分溶解度数据,请回答问题:
如表是KNO3、NaCl在不同温度下的部分溶解度数据,请回答问题:
(1)10℃时,KNO3溶解度是20.9g.
(2)40℃时,将70gKNO3固体加入100g水中,充分搅拌,形成的溶液质量为163.9g.
(3)60℃时,KNO3的饱和溶液中含有少量NaCl,通过降温结晶方法获得较纯净的KNO3晶体.
(4)t℃时,NaCl和KNO3的饱和溶液溶质质量分数相同,该温度范围是b.
a.10℃~20℃b.20℃~40℃c.40℃~60℃d.60℃~80℃
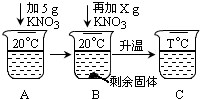
(5)向20mL水中溶解一定量KNO3固体的操作如图:请根据实验现象和溶解度数据回答:A、B、C中溶液一定不饱和溶液的是A.当x=1.32g时,B中恰好没有固体剩余.
 如表是KNO3、NaCl在不同温度下的部分溶解度数据,请回答问题:
如表是KNO3、NaCl在不同温度下的部分溶解度数据,请回答问题:| 温度(℃) | 10 | 20 | 40 | 60 | 80 |
| KNO3 | 20.9 | 31.6 | 63.9 | 110 | 169 |
| NaCl | 35.8 | 36 | 36.6 | 37.3 | 38.4 |
(2)40℃时,将70gKNO3固体加入100g水中,充分搅拌,形成的溶液质量为163.9g.
(3)60℃时,KNO3的饱和溶液中含有少量NaCl,通过降温结晶方法获得较纯净的KNO3晶体.
(4)t℃时,NaCl和KNO3的饱和溶液溶质质量分数相同,该温度范围是b.
a.10℃~20℃b.20℃~40℃c.40℃~60℃d.60℃~80℃
(5)向20mL水中溶解一定量KNO3固体的操作如图:请根据实验现象和溶解度数据回答:A、B、C中溶液一定不饱和溶液的是A.当x=1.32g时,B中恰好没有固体剩余.
3.“冰峰”、“肉夹馍”、“擀面皮”常被“老陕”称作“三秦套餐”.生产“冰峰”过程中用到了纯净水.纯净水属于( )
| A. | 混合物 | B. | 纯净物 | C. | 单质 | D. | 非金属单质 |
13.某同学欲测定一瓶标签残缺的硫酸镁溶液的溶质质量分数,取60g该溶液于烧杯中,向其中滴入足量的氢氧化钠溶液,记录有关数据如表:
反应的化学方程式为:MgSO4+2NaOH═Na2SO4+Mg(OH)2
(1)反应生成氢氧化镁沉淀的质量为2.9g;
(2)计算MgSO4溶液中溶质的质量分数10%(根据化学方程式计算);
(3)100g溶质质量分数为10%的NaOH溶液中氧元素的质量为84g.
| 反应前 | 反应后 | |
| 烧杯和硫酸镁溶液的质量 | 溶质质量分数为10%的NaOH溶液 | 过滤后烧杯和溶液总质量 |
| 80g | 100g | 177.1g |
(1)反应生成氢氧化镁沉淀的质量为2.9g;
(2)计算MgSO4溶液中溶质的质量分数10%(根据化学方程式计算);
(3)100g溶质质量分数为10%的NaOH溶液中氧元素的质量为84g.
20.某同学在一次化学实验中,不慎将盐酸滴到大理石的地面上,他看见地面上有气泡产生,该气体是 ( )
| A. | 氧气 | B. | 氢气 | C. | 二氧化碳 | D. | 二氧化硫 |
 如图为我国某次盛大集会上黑龙江省参展的彩车“龙腾盛世”,请按要求回答下列问题:
如图为我国某次盛大集会上黑龙江省参展的彩车“龙腾盛世”,请按要求回答下列问题: