题目内容
1.根据信息提示写出相应化学反应方程式:(1)生活中铝制品比铁制品更耐腐蚀,是因为铝在常温下即可形成一层致密的氧化物薄膜,写出此反应的化学反应方程式:4Al+3O2═2Al2O3.
(2)二氧化碳是一种宝贵的碳氧资源.在高温高压下以CO2和NH3为原料可以合成尿素[CO(NH2)2],同时有水生成.写出反应的化学方程式CO2+2NH3$\frac{\underline{\;高温、高压\;}}{\;}$CO(NH2)2+H2O.
(3)工业上利用海水提取溴(Br2),其主要反应之一是在一定条件下,将氯气通入浓缩的海水中,氯气与海水中的溴化钠反应得到溴.此反应的化学方程式为Cl2+2NaBr═2NaCl+Br2.
分析 根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式.
解答 解:(1)通常情况下,铝能和空气中的氧气反应生成氧化铝,反应的化学方程式为:4Al+3O2═2Al2O3;
(2)二氧化碳和氨气反应的化学方程式为:CO2+2NH3$\frac{\underline{\;高温、高压\;}}{\;}$CO(NH2)2+H2O;
(3)溴化钠和氯气反应的化学方程式为:Cl2+2NaBr═2NaCl+Br2.
故填:4Al+3O2═2Al2O3;CO2+2NH3$\frac{\underline{\;高温、高压\;}}{\;}$CO(NH2)2+H2O;Cl2+2NaBr═2NaCl+Br2.
点评 书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.

练习册系列答案
相关题目
12.下列应用及相应用化学方程式表示的原理及基本反应类型都正确的是( )
| A. | 煤炉里煤层上方发生的反应 C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 化合反应 | |
| B. | 加热高锰酸钾制氧气 KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ 分解反应 | |
| C. | 碳还原氧化铜 2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ 置换反应 | |
| D. | 家用天然气燃烧 CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$2H2O+CO2 氧化反应 |
9.天然淡水经过沉降(沉淀)、过滤、杀菌消毒等净化过程变成自来水,其中发生化学变化的是( )
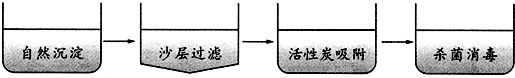

| A. | 自然沉淀 | B. | 沙层过滤 | C. | 活性炭吸附 | D. | 杀菌消毒 |
16.求KMnO4中锰元素的化合价是( )
| A. | +2 | B. | +3 | C. | +4 | D. | +7 |
6. A、B两种物质的溶解度曲线如下图所示.t3℃时,将A、B分别溶于100g水中,各自配成饱和溶液,然后降温.试根据溶解度曲线判断,下列说法正确的是( )
A、B两种物质的溶解度曲线如下图所示.t3℃时,将A、B分别溶于100g水中,各自配成饱和溶液,然后降温.试根据溶解度曲线判断,下列说法正确的是( )
 A、B两种物质的溶解度曲线如下图所示.t3℃时,将A、B分别溶于100g水中,各自配成饱和溶液,然后降温.试根据溶解度曲线判断,下列说法正确的是( )
A、B两种物质的溶解度曲线如下图所示.t3℃时,将A、B分别溶于100g水中,各自配成饱和溶液,然后降温.试根据溶解度曲线判断,下列说法正确的是( )| A. | t3℃时,两种饱和溶液中溶质的质量分数相等 | |
| B. | 降至t2℃时,A物质的溶液仍是饱和溶液 | |
| C. | 降至t1℃时,B物质的溶液里溶质的质量分数变小 | |
| D. | 降至t1℃时,两种溶液的质量均不变 |
10.鉴别稀盐酸和稀硫酸可选用的试剂是( )
| A. | Fe(OH)3 | B. | 紫色石蕊试液 | C. | CuO | D. | Ba(OH)2 |
