题目内容
13.一生锈的铁钉放到足量的稀HCl中,铁锈逐渐溶解生成黄色溶液,反应方程式Fe2O3+6HCl═2FeCl3+3H2O,之后又有气体产生,反应方程式Fe+2HCl═FeCl2+H2↑.分析 铁锈的主要成分是氧化铁,能与盐酸反应生成氯化铁与水,铁锈完全消失后,铁与稀盐酸反应生成氯化亚铁和氢气,据此写出反应的化学方程式即可.
解答 解:铁锈的主要成分是氧化铁(Fe2O3),将生锈的铁钉放入盐酸中,先是表面的铁锈的主要成分氧化铁与盐酸反应生成氯化铁与水,反应现象为:铁锈逐渐消失,溶液由无色变成黄色,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O.
当铁锈完全反应后,铁与盐酸发生反应,生成氯化亚铁与氢气,会观察到有气泡产生,反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
故答案为:黄;Fe2O3+6HCl═2FeCl3+3H2O;Fe+2HCl═FeCl2+H2↑.
点评 本题难度不大,主要考查酸的化学性质,掌握铁锈的主要成分、酸的化学性质、化学方程式的书写等是正确解答本题的关键.

练习册系列答案
相关题目
1.某同学的化学实验报告中有如下记录,其中合理的是( )
| A. | 用10毫升量筒量取8.2毫升稀硫酸溶液 | |
| B. | 用水银温度计测得某溶液的温度为20.54℃ | |
| C. | 用pH试纸测得某浓硫酸的pH值为1 | |
| D. | 用托盘天平称取17.14克氯化钠固体 |
18.下列化学方程式书写和反应类型标注都正确的是( )
| A. | CuO+CO═Cu+CO2↑ (置换反应) | |
| B. | 2KClO3 MnO2 $\frac{\underline{\;MnO_2\;}}{\;}$2KCl+3O2↑(分解反应) | |
| C. | CuSO4+Ba(OH)2═Cu(OH)2↓+BaSO4↓(复分解反应) | |
| D. | Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$MgO2 (化合反应) |
2.我国铁路将进入高铁时代.为适应提速要求需把短轨焊接连成长轨,常用反应:xAl+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+xFe进行焊接,该反应发生后,不需要再持续加热就可保持高温继续进行,方便野外操作.下列说法不正确的是( )
| A. | 该反应为置换反应 | B. | 该反应会放出大量热 | ||
| C. | Fe2O3为氧化物 | D. | 该反应方程式中的x为3 |
3.下列物质有刺激性气味的是( )
| A. | 氧气 | B. | 二氧化碳 | C. | 氨气 | D. | 氢气 |


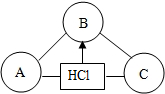 构建知识网络是一种重要的学习方法.右图是关于盐酸化学性质的知识网络,“-”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质.
构建知识网络是一种重要的学习方法.右图是关于盐酸化学性质的知识网络,“-”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质.