题目内容
5. NaOH是化学实验中常用的试剂.
NaOH是化学实验中常用的试剂.(1)将某NaOH溶液逐滴滴入一定量的稀盐酸中,右边图象合理的是乙(填“甲”或“乙”).
(2)向长期敞口放置的NaOH溶液中滴加盐酸时,意外发现有气泡产生,请写出此时溶液中一定存在的阴离子CO32-.
(3)向足量某NaOH溶液中通入CO2,反应后溶液中的溶质可能只有Na2CO3,也可能还有NaOH,请设计实验检验溶质的成分,简要写出实验步骤、现象和结论.(提示:Na2CO3溶液呈碱性)
分析 (1)将某NaOH溶液逐滴滴入一定量的某盐酸中,氢氧化钠与稀盐酸反应生成氯化钠和水,进行分析解答;
(2)氢氧化钠溶液能够吸收空气中的二氧化碳,并且能和二氧化碳反应生成碳酸钠和水;碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳;
(3)碳酸钠能和氯化钙反应生成碳酸钙和氯化钠,能和氯化钡(或氯化钙)溶液反应生成碳酸钡(碳酸钙)沉淀和氯化钠,氢氧化钠溶液显碱性,能使酚酞试液变红色.
解答 解:(1)将某NaOH溶液逐滴滴入一定量的某盐酸中,稀盐酸显酸性,pH小于7;氢氧化钠与稀盐酸反应生成氯化钠和水,完全反应时,溶液显中性,pH等于7;继续加入氢氧化钠溶液,溶液显碱性,pH大于7;pH值的变化是从小于7逐渐的增大到大于7,故所示图象合理的是乙.故填:乙;
(2)长期敞口放置的NaOH溶液,能与空气中的二氧化碳反应生成碳酸钠和水,碳酸钠能与稀盐酸反应生成氯化钠、水和二氧化碳,故会意外发现有气泡产生,碳酸钠是由钠离子与碳酸根离子构成的,其中的阴离子是碳酸根离子;故填:CO32-;
(3)向足量某NaOH溶液中通入CO2,反应后溶液中的溶质可能只有Na2CO3,也可能还有NaOH,请设计实验检验溶质的成分,设计的实验为:取反应后的溶液,加入足量氯化钡或氯化钙溶液,有白色沉淀生成,静置,取上层清液滴加酚酞试液,若溶液变红色,则溶质为碳酸钠和氢氧化钠;若溶液没有变成红色,则溶质只有碳酸钠;故答案为:取反应后的溶液,加入足量氯化钡(或氯化钙)溶液,有白色沉淀生成,静置,取上层清液滴加酚酞试液,若溶液变红色,则溶质为碳酸钠和氢氧化钠;若溶液没有变成红色,则溶质只有碳酸钠.
点评 本考点考查了碱的化学性质,解决本考点需要根据实验现象,综合分析,从而得出正确的结论.此考点主要出现在选择题和实验题中.

| 选项 | 甲 | 乙 | 丙 | 丁 |
| A | 氧化物 | NO | H2O2 | CuO |
| B | 污染物 | CO2 | PM2.5 | SO2 |
| C | 盐 | NaCl | K2CO3 | NaOH |
| D | 纯净物 | 空气 | 盐酸 | CaCO3 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 干冰 | B. | 天然气 | C. | 石油 | D. | 大理石 |
| A. | 干冰用作致冷剂-干冰是冰 | |
| B. | CO2含量过高导致人死亡-CO2有毒 | |
| C. | 用炭黑墨汁书写的字经久不变色-常温下,碳的化学性质稳定 | |
| D. | 制糖工业用活性炭脱色制白糖-活性炭和有色物质反应 |
| 蜡烛 | 装置Ⅱ | 装置Ⅲ | |
| 反应前的质量/g | 15.8 | 182.3 | 212.2 |
| 反应后的质量/g | 14.4 | 184.1 | 216.6 |
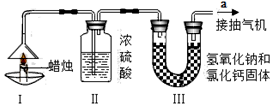
实验步骤如下:
①先分别称量蜡烛、装置Ⅱ(吸收水)、装置Ⅲ(吸收二氧化碳)的质量.②按图示连接好仪器,点燃蜡烛,同时从a导管口抽气.③一段时间后熄灭蜡烛,再分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量.
实验数据如上表.请回答:
①该实验中测得水的质量为1.8g.
②由该实验数据计算,蜡烛中碳、氢元素的质量之比为6:1.
③理论上,装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛失去的质量,其原因是与消耗的蜡烛比较,生成的二氧化碳和水中增加了参加反应的氧气所含氧元素质量.
④该实验能否准确测出蜡烛燃烧生成二氧化碳和水的质量?说明理由.
| A. | BaSO4→Ba(NO3)2 | B. | H2SO4→CuSO4 | C. | Na2CO3→NaOH | D. | Fe(OH)2→FeSO4 |
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | 稀盐酸 | 氯化钠 | 加入适量的氢氧化钠溶液 |
| B | 铜粉 | 铁粉 | 加入足量的稀盐酸溶解、过滤、洗涤 |
| C | 二氧化碳 | 一氧化碳 | 点燃 |
| D | 三氯化铁溶液 | 氯化铜 | 加入过量铁粉、过滤 |
| A. | A | B. | B | C. | C | D. | D |
| 物质 | 杂质 | 除杂质方法 | |
| ① | 氯化钠溶液 | 氢氧化钠 | 滴加稀盐酸至pH=7 |
| ② | 铁粉 | 铜粉 | 加入过量的稀盐酸 |
| ③ | 氨气 | 二氧化碳 | 将气体通过氢氧化钠溶液后干燥 |
| ④ | 二氧化碳 | 一氧化碳 | 通入氧气后点燃 |
| A. | ①② | B. | ①③ | C. | ②③ | D. | ③④ |