题目内容
8.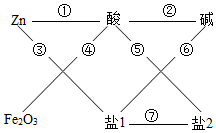 稀硫酸(H2SO4)、氢氧化钠(NaOH)、氯化钡(BaCl2)、硫酸铜(CuSO4)等溶液可参与如图所示的七大化学变化
稀硫酸(H2SO4)、氢氧化钠(NaOH)、氯化钡(BaCl2)、硫酸铜(CuSO4)等溶液可参与如图所示的七大化学变化(1)盐1是CuSO4.
(2)工业上,反应④的用途为除锈,该反应生成含铁的化合物的化学式是Fe2(SO4)3.
(3)不能用银替代图中的锌,其理由有二,理由之一是银的金属活动性弱不能与稀硫酸发生反应(或银的金属活动性弱不能置换硫酸铜中的铜).
(4)写出上述物质中发生中和反应的化学方程式是H2SO4+2NaOH=Na2SO4+2H2O.
分析 由于给出的是四种物质和图对应的关系,所以酸和碱是一定的,而给定物质中能和酸反应的盐是氯化钡即盐2为氯化钡,而和碱能反应的盐是硫酸铜即盐1为硫酸铜.因此可对应出物质之间的关系.
解答 解:
由于给出的酸碱各有一种,所以酸是硫酸,碱为氢氧化钠,而给定的两种盐只有氯化钡能和硫酸反应,而和碱反应的盐只是硫酸铜,所以转化关系为: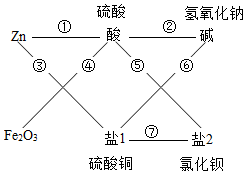
(1)盐1是 CuSO4.
(2)反应④是氧化铁和硫酸反应,生成硫酸铁和水,在工业上,反应④的用途为 除锈,该反应生成含铁的化合物的化学式是 Fe2(SO4)3.
(3)由于图中的锌既能和硫酸反应,也能和硫酸铜反应,而银活动性弱不能和稀硫酸反应,其活动性也比铜弱,所以也不能和硫酸铜反应,所以不能用银替代图中的锌,其理由有二,理由之一是 银的金属活动性弱不能与稀硫酸发生反应或银的金属活动性弱不能置换硫酸铜中的铜.
(4)中和反应是酸和碱反应生成盐和水,对应的是硫酸和氢氧化钠反应生成硫酸钠和水,对应的化学方程式为H2SO4+2NaOH=Na2SO4+2H2O.
故答案:
(1)CuSO4;
(2)除锈;Fe2(SO4)3;
(3)银的金属活动性弱不能与稀硫酸发生反应或银的金属活动性弱不能置换硫酸铜中的铜;
(4)H2SO4+2NaOH=Na2SO4+2H2O.
点评 结合给定物质的性质和转化关系进行物质的位置确定,然后结合给出的问题进行分析解答.

练习册系列答案
相关题目
18.如表列出了除去物质中所含少量杂质的方法,其中错误的是( )
| 选项 | 物质 | 杂质 | 除杂方法 |
| A | CO2 | CO | 点燃 |
| B | MnO2粉 | C粉 | 在空气中充分灼烧 |
| C | FeSO4溶液 | CuSO4溶液 | 加入足量的铁粉,过滤 |
| D | NaCl固体 | 泥沙 | 溶解、过滤 |
| A. | A | B. | B | C. | C | D. | D |
3.归纳与反思是学习化学的重要环节,下列各项归纳完全正确的一组是( )
| A、对性质和用途的认识 | B、资源的利用和保护 |
| ①一氧化碳有可燃性,可用于冶炼金属 ②石墨很软,可以制成电极 | ①爱护水资源要节约用水和防止水体污染 ②保护金属资源只能通过防止金属腐蚀实现 |
| C、“生活中安全”的措施 | D、用“化学”眼光分析 |
| ①在室内一盆水能防止煤气中毒 ②夜间发现液化气泄漏开灯寻找泄漏源 | ①洗涤剂去油污是因为起乳化作用 ②湿衣服晾干是因为分子不断运动 |
| A. | A | B. | B | C. | C | D. | D |
18.碳-14原子核中含6个质子与8个中子,生物体死亡后,体内含有的碳-14会逐渐减少(称为衰变),在衰变时,一个中子变成1个质子,形成新的原子核.因此科学家可通过测量生物体遗骸中碳-14的含量,来计算它存活的年代,这种方法称之为放射性碳测年法.下列关于衰变后的新原子核的说法正确的是( )
| A. | 碳原子核,含7个质子,8个中子 | B. | 氧原子核,含7个质子,8个中子 | ||
| C. | 碳原子核,含6个质子,7个中子 | D. | 氮原子核,含7个质子,7个中子 |
 往100g含有盐酸和氯化钙的混合溶液中,加入21.2%的碳酸钠溶液,所得溶液的pH变化与加入碳酸钠溶液的质量关系如图,试分析计算:
往100g含有盐酸和氯化钙的混合溶液中,加入21.2%的碳酸钠溶液,所得溶液的pH变化与加入碳酸钠溶液的质量关系如图,试分析计算: