题目内容
16. 红枣中含有丰富的VC和糖类,常食能增强人体的免疫力,有补血养气安神等良好功效,红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.某化学兴趣小组对一包久置的“504双吸剂”固体样品产生浓厚的兴趣,设计实验进行探究.
红枣中含有丰富的VC和糖类,常食能增强人体的免疫力,有补血养气安神等良好功效,红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.某化学兴趣小组对一包久置的“504双吸剂”固体样品产生浓厚的兴趣,设计实验进行探究.【提出问题】久置固体的成分是什么?
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【实验探究】甲同学的方案:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,滴加足量的稀盐酸 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有Fe, 一定不含Fe2O3. |
他设计如下实验方案继续验证.

(1)步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是增大接触面积,使得铁粉能够充分吸引;
(2)②中固体溶解时放出大量热,由此可以判断固体中一定含有CaO.
(3)③中反应的化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
乙同学对滤渣B又进行探究.
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失有气泡产生、澄清石灰水变浑浊,澄清石灰水变浑浊 溶液呈黄色. | 固体中一定含有CaCO3和Fe2O3. |
分析 本题探究了防腐剂的成分,取少量固体放于试管中,滴加足量的稀盐酸,固体逐渐消失,有大量无色气体产生,得到浅绿色溶液,固体中一定含有铁,不一定不含Fe2O3理由是:氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.
(1)由乙同学的设计方案可知:磁铁吸引了铁粉,②中固体溶解时放出大量热,因为生石灰溶于水生成熟石灰放出大量的热,由此可以判断固体中一定含有氧化钙;滤液A中的氢氧化钙和碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,配平即可;
对滤渣B又进行探究:①取滤渣B于试管中,加入适量稀盐酸,固体减少,有气泡冒出,溶液变为黄色;②将生成的气体通入澄清石灰水,澄清石灰水变浑浊;固体中一定含有CaCO3和Fe2O3.
解答 解:甲同学的方案:取少量固体放于试管中,滴加足量的稀盐酸,固体逐渐消失,有大量无色气体产生,得到浅绿色溶液,固体中一定含有铁.北北同学不一定不含Fe2O3理由是:氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.
(1)步骤①样品用磁铁吸引前需经过研碎,研碎的目的是 增大接触面积,使反应充分
(2)由乙同学的设计方案可知:磁铁吸引了铁粉,②中固体溶解时放出大量热,因为生石灰溶于水生成熟石灰放出大量的热,由此可以判断固体中一定含有氧化钙;反应的化学方程式为CaO+H2O=Ca(OH)2
(3)滤液A中的氢氧化钙和碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,化学方程式为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
对滤渣B的探究:①根据实验结论,固体中一定含有碳酸钙和氧化铁,因此取滤渣B于试管中,加入适量稀盐酸;②将生成的气体通入澄清石灰水,可看到固体减少,有气泡冒出,溶液变为黄色,澄清石灰水变浑浊;
故答案为:甲同学的方案:稀盐酸(或稀硫酸) Fe(或铁粉)
乙同学的理由:氧化铁与稀盐酸(或稀硫酸)反应生成的氯化铁(或硫酸铁)又与铁粉反应生成氯化亚铁(或硫酸亚铁).
(1)增大接触面积,使得铁粉能够充分吸引;
(2)CaO(或氧化钙);
(3)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
乙同学的探究:澄清石灰水变浑浊; 溶液呈黄色.
点评 有关实验方案的设计和对实验方案的评价是中考的热点之一,设计实验方案时,要注意用最少的药品和最简单的方法;关于对实验设计方案的评价,要在两个方面考虑,一是方案是否可行,能否达到实验目的;二是设计的方法进行比较,那种方法更简便.本考点主要出现在实验题中.

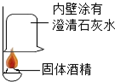 近几年餐饮行业经常使用一种“固体酒精”,替代相对不够安全的液体酒精,化学兴趣小组的同学对“固体酒精”产生了好奇,并对其成分进行研究.
近几年餐饮行业经常使用一种“固体酒精”,替代相对不够安全的液体酒精,化学兴趣小组的同学对“固体酒精”产生了好奇,并对其成分进行研究.【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成.
(2)氯化钙、氯化钡溶液均呈中性.
【提出问题】(1)酒精中是否含有碳元素?
(2)固体酒精中的氢氧化钠是否变质?
【实验探究】(1)按如图实验,发现澄清石灰水变浑浊,证明生成了CO2,可得出酒精中含有碳元素的结论.写出澄清石灰水变浑浊的化学方程式:CO2+Ca(OH)2=CaCO3↓+H2O
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀.取沉淀于试管中加稀盐酸,有气泡产生.分析实验并结合资料得出氢氧化钠已变质.①写出氢氧化钠变质的化学方程式:CO2+2NaOH=Na2CO3+H2O
②据上述信息写出产生沉淀的化学方程式:Na2CO3+CaCl2=CaCO3↓+2NaCl
(3)为进一步确定氢氧化钠的变质程度,分组探究.
| 方案 |  | 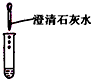 |
| 现象 | 溶液变红 | 产生白色沉淀 |
| 结论 | 溶液中有氢氧化钠 | 溶液中有碳酸钠 |
②乙组认为甲组实验不能证明清夜中一定有氢氧化钠,理由是碳酸钠溶液呈碱性,也能使酚酞溶液变红.他们另取烧杯中上层清夜,加足量氯化钡溶液,充分反应后滴加酚酞溶液,酚酞溶液变红.
【实验结论】经讨论一致认为固体酒精中的氢氧化钠部分变质.
【反思交流】乙组实验中加足量氯化钡溶液的目的是除去碳酸钠,防止影响对NaOH的检验
【拓展应用】要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC.
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液.

【提出问题】:常温下钠与氧气反应,产物有哪些?
【査阅资料】:钠的氧化物,除氧化钠(Na20)外还有过氧化钠(Na202),氧化钠与过氧化钠都能与水发生反应,方程式如下:
Na20+H20=2Na0H,2Na2O2+2H2O=4NaOH+O2↑
【作出猜想】:常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na202,
猜想3:Na2O和Na2O2
【实验探究一】:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | 猜想1正确 |
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验探究二】:
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量白色固体加入足量氯化钙溶液 | 产生白色沉淀 | 白色固体成分为Na2C03和 NaOH |
| 2.过滤、取少量滤液加入无色的酚酞试液 |
(1)类比氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式Na2O+2HCl=2NaCl+H2O.
(2)过氧化钠也能与盐酸反应,方程式为:2Na202+4HCl=4NaCl+2H2O+X,X的化学式为O2.
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2不是碱性氧化物(填“是”或“不是”).




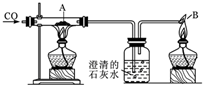 如图是实验室用CO还原Fe2O3的实验装置,请回答:
如图是实验室用CO还原Fe2O3的实验装置,请回答: