题目内容
15. 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.请仔细阅读后计算:
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.请仔细阅读后计算:(1)实验室欲配制200g质量分数为9.8%的稀硫酸备用,需要这种硫酸20g
(2)取(1)中配制好的硫酸溶液100g,向其中加入100g氢氧化钠溶液,充分反应后,测得溶液的pH=7,计算反应后所得溶液中溶质的质量分数.
分析 溶液稀释前后,溶质质量不变;
氢氧化钠和稀硫酸反应生成硫酸钠和水,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)设需要这种硫酸质量为x,根据题意有:x×98%=200g×9.8%,
x=20g,
故填:20.
(2)设生成硫酸钠质量为x,
2NaOH+H2SO4═Na2SO4+2H2O,
98 142
100g×9.8% x
$\frac{98}{100g×9.8%}$=$\frac{142}{x}$,
x=14.2g,
反应后所得溶液中溶质的质量分数为:$\frac{14.2g}{100g+100g}$×100%=7.1%,
答:反应后所得溶液中溶质的质量分数为7.1%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
5.一位农民种植的某块农田小麦产量总是比邻近地块的低.他怀疑该农田可能是缺少某种元素,为此将该块肥力均匀的农田分成面积相等的五小块,进行田间实验.除施肥不同外,其他田间处理措施相同.实验结果如下表,从表中可判断,该农田最可能缺少的元素是( )
| 地 块 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 施 肥 情 况 | 尿素 CO(NH2)2 | 磷酸二氢钾 KH2PO4 | 磷酸二氢铵 NH4H2PO4 | 硫酸铵 (NH4)2SO4 | 不施肥 |
| 小麦收获量 | 55.56 | 70.26 | 56.88 | 55.44 | 55.11 |
| A. | K | B. | N | C. | P | D. | S |
6.向硝酸银、硝酸铜、硝酸镁的混合液中加入一些铁粉,待完全反应后,再过滤.下列情况不可能存在的是( )
| A. | .滤纸上有Ag,滤液中有Ag+、cu2+、Fe2+、Mg2+ | |
| B. | .滤纸上有Ag、Cu,滤液中有Ag+、Fe2+、Mg2+ | |
| C. | 滤纸上有Ag、Cu,滤液中有Fe2+、Mg2+ | |
| D. | .滤纸上有Ag、Cu、Fe,滤液中有Fe2+、Mg2+ |
3.下述氮肥的每吨市场价格如下:CO(NH2)2:1080元;(NH4)2SO4:450元;NH4NO3:810元;NH4HCO3:330元.分别用m元钱采购上述氮肥,购得的氮肥含氮元素最多的是( )
| A. | CO(NH2)2 | B. | (NH4)2SO4 | C. | NH4NO3 | D. | NH4HCO3 |
20.现在越来越多的人喜欢喝茶,茶叶中含有茶氨酸(C7H14O3N2)具有降血压、提高记忆力、保护神经细胞、减肥等功效,下列有关茶氨酸的说法正确的是( )
| A. | 茶氨酸是由多种原子构成的化合物 | B. | 茶氨酸中碳、氮元素的质量比为7:2 | ||
| C. | 茶氨酸中含有氮原子 | D. | 茶氨酸由C、H、N、O四种元素组成 |
4.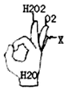 如图是某同学用OK手势表示初中化学反应中生成水的不同方法,手指上的物质通过某种反应可直接生成水(如图中的H2O2、O2),则物质X一定不是( )
如图是某同学用OK手势表示初中化学反应中生成水的不同方法,手指上的物质通过某种反应可直接生成水(如图中的H2O2、O2),则物质X一定不是( )
 如图是某同学用OK手势表示初中化学反应中生成水的不同方法,手指上的物质通过某种反应可直接生成水(如图中的H2O2、O2),则物质X一定不是( )
如图是某同学用OK手势表示初中化学反应中生成水的不同方法,手指上的物质通过某种反应可直接生成水(如图中的H2O2、O2),则物质X一定不是( )| A. | CuO | B. | CO | C. | CH4 | D. | H2CO3 |
5.下列物质的用途,利用其物理性质的是( )
| A. | 干冰用于人工降雨 | B. | 小苏打治疗胃酸过多 | ||
| C. | 稀硫酸用于金属除锈 | D. | 氦气常用作保护气 |