题目内容
15. 用如图的实验装置来探究水的组成,说法正确的是( )
用如图的实验装置来探究水的组成,说法正确的是( )| A. | a试管内的气体可以使带火星的木条复燃 | |
| B. | 反应产生的氢气和氧气的体积比为1:2 | |
| C. | 在水中少量硫酸钠或氢氧化钠是为了增强水的导电性 | |
| D. | 通过该实验可以得出水是由2个氢原子和1个氧气构成的 |
分析 根据电解水的实验现象和结论回答:电解水时正极生成的是氧气,负极生成的是氢气,电解水实验说明水是由氢元素和氧元素组成的.
解答 解:A、由电解水的装置可知,a试管内的气体可是电源的负极产生的气体是氢气,不能使带火星的木条复燃.故A错误;
B、电解水时产生的氢气和氧气的体积比为2:1,故B错误;
C、在水中少量硫酸钠或氢氧化钠是为了增强水的导电性,故C正确;
D、通过该实验可以得出水是由氢元素和氧元素组成的,故D错误.
故选C.
点评 本题的难度不大,熟记电解水实验的现象、结论即可分析解答.

练习册系列答案
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
10.从中药材青蒿中提取的青蒿素被世界卫生组织认为是“世界上唯一有效的疟疾治疗药物”我国科学家屠呦呦因为对青蒿素的研究做出突出贡献,获得2105年诺贝尔生理医学奖,是第一个获得诺贝尔自然学奖的中国人,青蒿素的化学式为C15H22O5关于青蒿素的说法错误的是( )
| A. | 青蒿素是由碳、氢、氧元素组成的 | |
| B. | 青蒿素中氧元素的质量分数约为28.4% | |
| C. | 青蒿素中有15个碳原子、22个氢原子、5个氧原子 | |
| D. | 青蒿素的燃烧产物中可能有二氧化碳和水 |
20.以下关于碳的性质说法正确的是( )
| A. | 需要长时间保存的档案都用碳素笔来填写,是因为碳的化学性质稳定 | |
| B. | 碳和氧气反应产物只有二氧化碳 | |
| C. | 所有的碳单质都是黑色的 | |
| D. | 活性炭可还原氧化铜 |
5.氧气在放电的条件下可以转化为臭氧(O3).下列说法中正确的是( )
| A. | 该变化是物理变化 | B. | 臭氧与氧气含有的元素相同 | ||
| C. | 臭氧与氧气的物理性质相同 | D. | 臭氧是一种新型的化合物 |

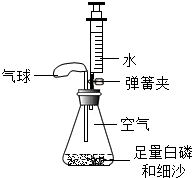 某实验小组利用如图所示装置测量空气中氧气的体积分数并取得成功.
某实验小组利用如图所示装置测量空气中氧气的体积分数并取得成功.