题目内容
3.酸具有通性的原因是( )| A. | 酸都能电离出H+ | B. | 酸都含有酸根 | ||
| C. | 酸中都含有氢元素 | D. | 酸中都含有氧元素 |
分析 根据酸是电离时产生的阳离子全部是氢离子的化合物,据此进行分析判断即可.
解答 解:A、酸溶液具有相似化学性质的原因是在水溶液中都能电离出氢离子,故选项正确.
B、酸溶液具有相似化学性质的原因是在水溶液中都能电离出氢离子,而不是含有酸根,故选项错误.
C、酸溶液具有相似化学性质的原因是在水溶液中都能电离出氢离子,而不是酸中都含有氢元素,故选项错误.
D、酸溶液具有相似化学性质的原因是在水溶液中都能电离出氢离子,而不是酸中都含有氧元素,故选项错误.
故选:A.
点评 本题难度不大,主要考查了酸具有相似化学性质的原因(阳离子全部是氢离子)是正确解答本题的关键.

练习册系列答案
相关题目
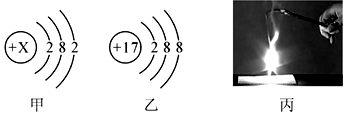
18.如图表示某化学反应的微观过程,有关该反应的说法正确的是( )

| A. | 该反应属于复分解反应 | |
| B. | 反应前后分子种类和数目不变 | |
| C. | 甲物质中氮、氧元素的质量比为1:3 | |
| D. | 参加反应甲、乙物质的分子个数比为4:5 |
8.要除去下列四种物质中的少量杂质(括号内的物质为杂质)
甲:CaCO3 (Na2CO3) 乙:NaOH (Na2CO3) 丙:NaCl (NaHCO3) 丁:炭粉(CuO)
可选用的试剂及操作方法有:①加适量盐酸,搅拌,过滤,洗涤;②加适量水,搅拌,过滤;③加适量盐酸,蒸发;④溶解,加适量石灰水,过滤,蒸发.下列组合正确的是( )
甲:CaCO3 (Na2CO3) 乙:NaOH (Na2CO3) 丙:NaCl (NaHCO3) 丁:炭粉(CuO)
可选用的试剂及操作方法有:①加适量盐酸,搅拌,过滤,洗涤;②加适量水,搅拌,过滤;③加适量盐酸,蒸发;④溶解,加适量石灰水,过滤,蒸发.下列组合正确的是( )
| A. | 甲-②,乙-④ | B. | 乙-③,丙-① | C. | 丙-①,丁-② | D. | 丁-③,丙-② |
13.下面是某化学反应的微观模型示意图,据此分析错误的是( )
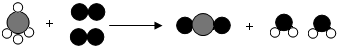

| A. | 反应前后原子数目没有变化 | |
| B. | 化学反应的本质是原子的重新组合过程 | |
| C. | 分子的种类发生变化 | |
| D. | 示意图中的各物质均属于化合物 |
 金属与盐溶液的反应遵循金属活动性顺序:
金属与盐溶液的反应遵循金属活动性顺序: