题目内容
某同学用高锰酸钾制氧气,取31.6g高锰酸钾放入试管中加热,一段时间后停止加热,称量试管中固体的质量是28.4g.请计算:
(1)该同学制得的氧气是 g.
(2)理论上可回收二氧化锰的质量是多少?
【考点】根据化学反应方程式的计算.
【专题】有关化学方程式的计算;有关化学方程式的计算.
【分析】(1)根据质量守恒定律,求出生成氧气的质量;
(2)根据生成氧气的质量,利用反应的化学方程式,得出各物质之间的质量比,列出比例式,即可计算出回收二氧化锰的质量.
【解答】解:(1)根据质量守恒定律,当固体质量变为28.4g时,生成氧气的质量为31.6g﹣28.4g=3.2g.
(2)设生成MnO2的质量为x
2KMnO4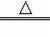
 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
87 32
x 3.2g
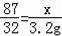

x=8.7g
答案:(1)3.2;(2)回收二氧化锰的质量为8.7g.
【点评】本题主要考查学生对化学反应方程式的书写,以及运用方程式进行计算的能力.

某方便面的营养成分表如下(其中碳水化合物主要指淀粉等):
| 营 养 成 分 表 |
| 项目 每100克 |
| 能量 1966千焦 蛋白质 7.5克 脂肪 21.8克 碳水化合物 60.7克 钠 2530毫克 |
(1)表中“钠”是指 (填序号).
A.离子 B.分子 C.元素 D.单质
(2)方便面中含的营养素有 种。
(3)方便面中使用的食盐可以是加碘盐,人体中缺碘可能患有的疾病是 (填“甲状腺肿大”或“骨质疏松”)。
(4)若小明用天然气煮方便面,请问天然气主要成份燃烧的化学方程式是 。
(5)若用漏勺捞煮好的方便面,与化学基本操作中的 原理相似。
(6)中国居民膳食指南建议每天食用食盐不超过6克。假设小明某天吃了100克该方便面,相当于吃了食盐 克(保留小数点后一位)。
一定条件下,甲、乙、丙、丁四种物质在一密闭容器中充分反应,测得反应前后各物质的质量如下表,有关说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 2 | 8 | 30 | 50 |
| 反应后质量/g | 20 | 待测 | 46 | 16 |
A.该反应类型为化合反应
B.待测值为0
C.反应中甲和丙的质量比为9﹕8
D.乙一定是该反应的催化剂
铜铝复合粉末被认为 在固体火箭推进剂领域有广泛的应用前景.现有铜粉、铝粉的混合物,请设计实验除去其中的铝粉并得到干燥的铜粉.
在固体火箭推进剂领域有广泛的应用前景.现有铜粉、铝粉的混合物,请设计实验除去其中的铝粉并得到干燥的铜粉.
| 混合物 | 主要操作步骤 | 相关的化学方程式 |
| 铜(Al) |
|
|
 要对库内气体取样检验。现有可选用的实验仪器如下:橡皮管、集气瓶、玻璃片、盛满水的水槽、烧杯和漏斗。你怎样用最简单的方法取出仓库内气体的样品?
要对库内气体取样检验。现有可选用的实验仪器如下:橡皮管、集气瓶、玻璃片、盛满水的水槽、烧杯和漏斗。你怎样用最简单的方法取出仓库内气体的样品?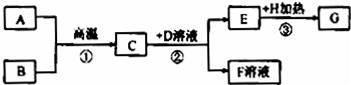

 B.
B. C.
C. D.
D.
