题目内容
16. 同学们知道铁的化学性质比较活泼,能与多种物质发生化学反应.化学兴趣小组的同学在课外资料中发现,铁和氧化铁竟然也能发生化学反应.
同学们知道铁的化学性质比较活泼,能与多种物质发生化学反应.化学兴趣小组的同学在课外资料中发现,铁和氧化铁竟然也能发生化学反应.【提出问题】铁和氧化铁反应的产物是什么?
【查阅资料】铁的氧化物有氧化铁、氧化亚铁、四氧化三铁.其中,只有氧化铁是红棕色,其余皆是黑色;只有氧化亚铁在空气中会很快被氧化成氧化铁;只有四氧化三铁有磁性.另外,二氧化碳不与铁反应,也不与铁的氧化物反应.
【猜想与假设】根据质量守恒定律,请你猜想该反应的产物:
①只有氧化亚铁; ②只有四氧化三铁; ③氧化亚铁和四氧化三铁
【进行实验】
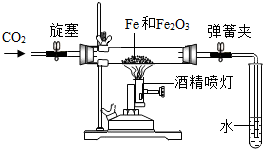
(1)按如图连接好仪器,检查装置的气密性.
(2)将足量的铁粉与适量的氧化铁粉末混合,装入玻璃管.轻轻打开旋塞,通入干燥、纯净的二氧化碳.过一会儿后,关闭旋塞.
(3)点燃酒精喷灯加热药品2~3min,粉末全部变黑;此时先将弹簧夹夹在橡皮管上,再停止加热;等到玻璃管冷却至室温,倒出黑色粉末,然后检验.
(4)检验黑色粉末的操作如下,请你完成其中的空白:
| 序号 | 操作及现象 | 结论 |
| a | 黑色粉末暴露在空气中不变色,用磁铁 靠近,能完全被吸引 | 黑色粉末中一定没有氧化亚铁 猜想①③错误 |
| b | 取少量的黑色粉末装入试管,滴加足量 硫酸铜溶液,出现红色固体,充分反 应后仍残留黑色固体 | 黑色粉末中一定含有铁和四氧化三铁 猜想②正确 |
【反思与评价】
(1)在实验操作第(2)步,通入CO2的目的是排出玻璃管中的空气,防止高温时铁被空气中的氧气氧化.
(2)在实验操作第(3)步,为什么要先夹上弹簧夹后再停止加热.防止试管中的水倒流入玻璃管.
(3)实验中盛水的试管里发生反应的化学方程式是CO2+H2O═H2CO3.
分析 【猜想与假设】
根据质量守恒定律,该反应的产物可能只有氧化亚铁;可能只有四氧化三铁; 可能是氧化亚铁和四氧化三铁;
【进行实验】
铁能和硫酸铜反应生成硫酸亚铁和铜;
【探究结论】
铁和氧化铁会发生化合反应生成四氧化三铁;
【反思与评价】
高温条件下,铁能和空气中的氧气反应;
不同的实验装置,功能不同;
二氧化碳和水反应生成碳酸.
解答 解:【猜想与假设】
根据质量守恒定律,该反应的产物可能只有氧化亚铁;可能只有四氧化三铁; 可能是氧化亚铁和四氧化三铁.
故填:氧化亚铁和四氧化三铁.
【进行实验】
(4)检验黑色粉末的操作如下表所示:
| 序号 | 操作及现象 | 结论 |
| a | 黑色粉末暴露在空气中不变色,用磁铁 靠近,能完全被吸引 | 黑色粉末中一定没有氧化亚铁 猜想①③错误 |
| b | 取少量的黑色粉末装入试管,滴加足量硫酸铜溶液,出现红色固体,充分反 应后仍残留黑色固体 | 黑色粉末中一定含有铁和四氧化三铁 猜想②正确 |
铁和氧化铁会发生化合反应生成四氧化三铁,反应方程式是:Fe+4Fe2O3$\frac{\underline{\;高温\;}}{\;}$ 3Fe3O4.
故填:Fe+4Fe2O3$\frac{\underline{\;高温\;}}{\;}$ 3Fe3O4.
【反思与评价】
(1)在实验操作第(2)步,通入CO2的目的是排出玻璃管中的空气,防止高温时铁被空气中的氧气氧化.
故填:排出玻璃管中的空气,防止高温时铁被空气中的氧气氧化.
(2)在实验操作第(3)步,要先夹上弹簧夹后再停止加热,这样能够防止试管中的水倒流入玻璃管,从而防止炸裂玻璃管.
故填:防止试管中的水倒流入玻璃管.
(3)实验中盛水的试管里,二氧化和水反应生成碳酸,发生反应的化学方程式为:CO2+H2O═H2CO3.
故填:CO2+H2O═H2CO3.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
6.下列物质的用途,主要利用其化学性质的是( )
| A. | 金刚石用来裁玻璃 | B. | 干冰用于人工降雨 | ||
| C. | 乙醇被用作内燃机中的燃料 | D. | 铝用于制造电线 |
7.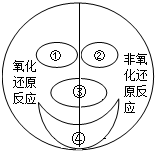 有元素化合价变化的反应是氧化还原反应:没有元素化合价变化的反应是非氧化还原反应,初中化学所学的四种化学反应类型与它们的关系如图所示,下列推断正确的是( )
有元素化合价变化的反应是氧化还原反应:没有元素化合价变化的反应是非氧化还原反应,初中化学所学的四种化学反应类型与它们的关系如图所示,下列推断正确的是( )
 有元素化合价变化的反应是氧化还原反应:没有元素化合价变化的反应是非氧化还原反应,初中化学所学的四种化学反应类型与它们的关系如图所示,下列推断正确的是( )
有元素化合价变化的反应是氧化还原反应:没有元素化合价变化的反应是非氧化还原反应,初中化学所学的四种化学反应类型与它们的关系如图所示,下列推断正确的是( )| A. | ①肯定是置换反应 | B. | ②肯定是分解反应 | ||
| C. | ③肯定是化合反应 | D. | ④肯定是复分解反应 |
4.除去下列各物质中混有的少量杂质,所用方法不正确的是( )
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | FeCl2溶液(ZnCl2) | 加足量铁粉,过滤 |
| B | C(CuO) | 加入足量盐酸、过滤、洗涤干燥 |
| C | NaCl溶液(MgSO4) | 加入适量的氯化钡溶液、过滤 |
| D | H2(HCl) | 通过足量氢氧化钠溶液,再干燥 |
| A. | A | B. | B | C. | C | D. | D |
5.将一定量的氢氧化钠和氯化铵固体混合物加热,测得反应前后各物质的质量如下表.
①表中a的值为2.8②X不一定是化合物③X中一定含有氢元素④X可能是该反应的催化剂⑤X的相对分子质量为17⑥X中一定含氢、氮元素,其质量比为2:7⑦X中氮元素的质量分数约为82.4%,对以上说法判断正确的是( )
| 物质 | NaOH | NH4Cl | NaCl | H2O | X |
| 反应前质量/g | 8.0 | 10.7 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 11.7 | 3.6 | a |
| A. | ①②③正确 | B. | 只有⑤⑦正确 | C. | 只有⑥③正确 | D. | 只有①⑦正确 |
6.茶叶中含有茶氨酸(C7H14O3N2,又称谷氨酸乙胺),它有降低血压,提高记忆力,保护伸进细胞、减肥等效果,下列有关它的说法中,正确的是( )
| A. | 茶氨酸中由C、H、O、N四种元素组成 | B. | 茶氨酸的相对分子质量为174 | ||
| C. | 茶氨酸中氧元素的质量分数为12% | D. | 茶氨酸中有1个氮分子 |
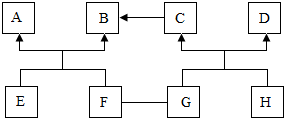 A-H是初中化学常见的化合物,且分别是由H、O、S、Na、Ca、Cu中的两种或三种元素组成的.其中B、E是氧化物,E中两种元素质量之比为2:3,C、F、H为相同类别的化合物,F易溶于水并放出大量的热,G的溶液呈蓝色,图中“--”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系,部分反应物、生成物或反应条件已略去.
A-H是初中化学常见的化合物,且分别是由H、O、S、Na、Ca、Cu中的两种或三种元素组成的.其中B、E是氧化物,E中两种元素质量之比为2:3,C、F、H为相同类别的化合物,F易溶于水并放出大量的热,G的溶液呈蓝色,图中“--”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系,部分反应物、生成物或反应条件已略去.
 根据如图所示信息判断,下列关于铝的说法正确的是B
根据如图所示信息判断,下列关于铝的说法正确的是B