题目内容
6.某化学兴趣小组为测定制二氧化碳用的大理石的纯度,进行如图所示的实验.请计算(假设大理石中的杂质不与稀盐酸反应,溶于水中的二氧化碳忽略不计)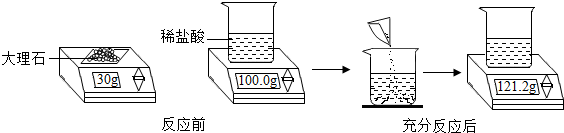
(1)反应后生成二氧化碳的质量为8.8g
(2)该大理石中碳酸钙的纯度是多少?(准确至0.1%)
分析 (1)根据质量守恒定律可知烧杯内质量的减少量就是生成二氧化碳的质量;
(2)根据二氧化碳的质量算出碳酸钙的质量,再除以样品的质量即可.
解答 解:(1)根据质量守恒定律,产生CO2的质量的为(100g+30g)-121.2g=8.8g
(2)设:大理石样品中碳酸钙的质量为x.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 8.8g
则$\frac{100}{44}=\frac{x}{8.8g}$,解得x=20g
大理石样品中碳酸钙的质量分数为:$\frac{20}{30}$×100%≈66.7%
答:大理石样品中碳酸钙的质量分数为66.7%.
故答案为:(1)20g;(2)66.7%.
点评 解答本题的关键是根据质量守恒定律可知烧杯内质量的减少量就是生成二氧化碳的质量,根据二氧化碳的质量再计算碳酸钙的质量即可.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
14.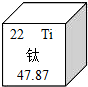 钛被誉为“未来金属”,在航天、航空、精密仪器等方面有广阔前景.如图是钛元素在元素周期表中的信息.则下列说法正确的是( )
钛被誉为“未来金属”,在航天、航空、精密仪器等方面有广阔前景.如图是钛元素在元素周期表中的信息.则下列说法正确的是( )
 钛被誉为“未来金属”,在航天、航空、精密仪器等方面有广阔前景.如图是钛元素在元素周期表中的信息.则下列说法正确的是( )
钛被誉为“未来金属”,在航天、航空、精密仪器等方面有广阔前景.如图是钛元素在元素周期表中的信息.则下列说法正确的是( )| A. | 钛元素的相对原子质量为47.87g | B. | 钛是非金属 | ||
| C. | 钛原子核内有22个质子 | D. | 钛的化学式为Ti2 |
1.人类和日常生活离不开谁,下列做法中,不利于节约用水的是( )
| A. | 用淘米水浇花 | B. | 洗碗筷时用水盆盛水清洗 | ||
| C. | 园林工人采用滴灌的方式浇灌花草 | D. | 洗手打肥皂时不关水龙头 |
11.按氧化物,酸,碱,盐的顺序排列的一组物质是( )
| A. | H2SO4,Na2CO2,NaCl,CuO | B. | H2O,HCl,Ca(OH)2,Na2SO4 | ||
| C. | H2SO4,NaOH,Na2CO3,Fe2O3 | D. | NaOH,H2CO3,NaCl,CO2 |
18.如图表示治理汽车尾气所涉及反应的微观过程.下列说法不正确的是( )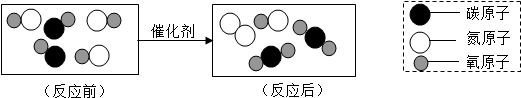

| A. | 图中单质的化学式为N2 | B. | 反应使有害气体转化为无害气体 | ||
| C. | 反应前后原子个数相等 | D. | 生成单质与化和物的质量比为7:21 |
15.下表列出了除去物质中所含少量杂质的方法,其中不正确的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | N2 | O2 | 将气体缓缓通过足量的灼热铜网 |
| B | NaCl溶液 | Na2SO4 | 溶解,加入适量硝酸钡溶液过滤 |
| C | Cu(NO3)2溶液 | AgNO3 | 加入足量铜粉,充分反应后过滤 |
| D | CaCl2溶液 | HCl | 加入足量碳酸钙粉末,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
16.下列知识整理的内容有错误的是( )
| A.实验方法 | B.化学与生活 |
| ①鉴别O2、CO2--可用澄清石灰水 ②熄灭酒精灯--用嘴吹灭 ③除去水瓶中的水垢--用稀盐酸 | ①人体缺铁会引起贫血症 ②进入久未开启的菜窖时先做灯火实验 ③用活性炭净水器可净化水 |
| C.实验记录 | D.物质构成 |
| ①用10ml量筒量取8ml 水 ②滴有紫色石蕊试液的水中通入CO2后变红 ③用托盘天平称取5.6g食盐 | ①分子、原子、离子都是构成物质的微粒 ②空气、液氧、二氧化硫中都含有氧分子 ③碳酸钠的化学式为NaCO3 |
| A. | 实验方法 | B. | 化学与生活 | C. | 实验记录 | D. | 物质构成 |