题目内容
8.在托盘天平的左右两托盘中各放置一只烧杯,调节天平使之平衡,向烧杯中分别注入足量且等质量、等浓度的稀硫酸,然后向两只烧杯中分别加入相同质量的锌片和铁银合金片,反应完成后天平仍保持平衡.则合金中铁和银的质量比为56:9.分析 该题目将化学反应与托盘天平平衡结合在一起.两盘中酸和金属质量相等,完全反应,天平仍平衡则产生氢气相等.由氢气质量求出反应的铁和锌的质量进而求出银的质量.
解答 解:设产生氢气的质量为2g,需要锌的质量为x,需要铁的质量为y,则有
Zn+H2SO4═ZnSO4+H2↑
65 2
x 2g
$\frac{65}{2}=\frac{x}{2g}$
x=65g
Fe+H2SO4═FeSO4+H2↑
56 2
y 2g
$\frac{56}{2}=\frac{y}{2g}$
y=56g
铁银合金的质量与锌的质量相等,故银的质量为65g-56g=9,所以铁和银的质量比为56:9.
故填:56:9.
点评 金属与酸反应后天平平衡的问题是中考常考查的题目,完成此类题目,要分清题干提供的信息,确定是根据酸还是金属的质量进行求算.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
13.溶液与人类的生活息息相关,溶液的配制是日常生活中和化学实验中常见的操作,下表中是硫酸溶液和氨水的密度与其溶质的质量分数对照表(20℃).请仔细分析列式计算:
(1)取12%的硫酸溶液100毫升可配制成6%的溶液多少克
(2)向200毫升28%的氨水中加入240毫升水,摇匀,溶液的体积是多少毫升?(结果保留一位小数)
| 溶液中溶质的质量分/% | 4 | 12 | 16 | 24 | 28 |
| 硫酸溶液的密度/(g/mL) | 1.02 | 1.08 | 1.11 | 1.17 | 1.20 |
| 氨水的密度/(g/mL) | 0.98 | 0.95 | 0.94 | 0.91 | 0.90 |
(2)向200毫升28%的氨水中加入240毫升水,摇匀,溶液的体积是多少毫升?(结果保留一位小数)
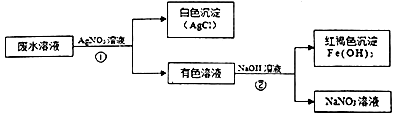
 如图是初中化学中常见物质间的转化关系,其中甲、乙、丙均为非金属单质;A、B、E和丁均为化合物;B和E为能产生温室效应的气体;乙和丁为黑色固体.
如图是初中化学中常见物质间的转化关系,其中甲、乙、丙均为非金属单质;A、B、E和丁均为化合物;B和E为能产生温室效应的气体;乙和丁为黑色固体.
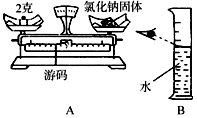 实验室欲配制100克溶质质量分数为10%的氯化钠溶液,请回答下列问题:
实验室欲配制100克溶质质量分数为10%的氯化钠溶液,请回答下列问题: