题目内容
17.下列说法正确的是( )| A. | K2MnO4、KMnO4、MnO2三者中Mn元素的化合价逐渐升高 | |
| B. | 金、银、铜金属活动性顺序逐渐减弱 | |
| C. | NH4NO3、NaCl、CaO三者溶于水后,所得溶液的温度逐渐降低 | |
| D. | NaOH、NaCl、H2SO4三者溶液的pH逐渐变小 |
分析 A、根据在化合物中正负化合价代数和为零进行分析;
B、根据金属的活动性进行分析;
C、根据物质溶于水后温度的变化进行分析;
D、根据物质溶液的pH的酸碱度的强弱进行分析.
解答 解:A、钾显+1价,氧显-2价,根据在化合物中正负化合价代数和为零可知,K2MnO4、KMnO4、MnO2三者中Mn元素的化合价依次为+6、+7、+4,故说法错误;
B、金、银、铜金属活动性由强到弱是铜、银、金,故说法错误;
C、NH4NO3溶于水温度降低;NaCl溶于水温度基本不变;CaO和水反应放出大量的热,温度升高,因此三者溶于水后,所得溶液的温度逐渐升高,故说法错误;
D、H2SO4显酸性,NaCl溶液显中性,NaOH溶液显碱性,因此三者溶液的pH逐渐变小,故说法正确;
故选:D.
点评 本题难度不大,掌握元素化合价的计算方法、溶液的酸碱性以及金属的活动性强弱等是解决此题的关键.

练习册系列答案
 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
7.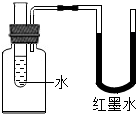 如图所示,向试管中加入某不与水反应的物质后,右边液面降低些,左边液面升高了些,则加入的物质可能是( )
如图所示,向试管中加入某不与水反应的物质后,右边液面降低些,左边液面升高了些,则加入的物质可能是( )
 如图所示,向试管中加入某不与水反应的物质后,右边液面降低些,左边液面升高了些,则加入的物质可能是( )
如图所示,向试管中加入某不与水反应的物质后,右边液面降低些,左边液面升高了些,则加入的物质可能是( )| A. | 活性炭 | B. | 氯化钠 | C. | 氢氧化钠 | D. | 硝酸铵 |
8.如表是生活中一些物质的pH:
有关它们的说法中正确的是( )
| 物质种类 | 厕所清洁剂 | 桔子汁 | 牛奶 | 草木灰水 | 厨房清洁剂 |
| pH | 1 | 3 | 6.5 | 11 | 12.5 |
| A. | 牛奶的酸性比桔子汁强 | |
| B. | 胃酸过多的人不宜多吃桔子 | |
| C. | 草木灰水显酸性 | |
| D. | 用湿润的pH试纸蘸取厕所清洁剂测其pH |
5.如图是氟元素在元素周期表中的有关信息和核外电子排布示意图,下列说法正确的是( )


| A. | 氟元素属于金属元素 | B. | 一个氟原子的质量是19.00g | ||
| C. | 氟在反应中易失去一个电子 | D. | 一个氟原子的原子核外有9个电子 |
12.A在B中充分燃烧生成C和D,A、B、C、D的微观示意图如下所示.
(1)一个A分子中共有4个原子,A物质中碳元素和氢元素质量比为14:3.
(2)写出A在B中完全燃烧生成C和D的化学方程式4NH3+3O2$\frac{\underline{\;一定条件\;}}{\;}$2N2+6H2O.
(3)上述四种物质中,属于氧化物的是C(填字母序号).
| 物质 | A | B | C | D |  |
| 分子示意图 |  |  |  |  |
(2)写出A在B中完全燃烧生成C和D的化学方程式4NH3+3O2$\frac{\underline{\;一定条件\;}}{\;}$2N2+6H2O.
(3)上述四种物质中,属于氧化物的是C(填字母序号).
6.如图表示初中化学常见实验操作,其中正确的是( )
| A. | 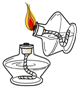 点燃酒精灯 | B. | 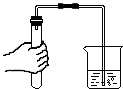 检查装置的气密性 | ||
| C. |  读出液体的体积 | D. | 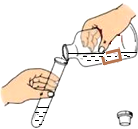 液体的取用 液体的取用 |
11.2016年3月份的两会呼吁每一位公民从自身开始,采取实际行动,应对当前中国最紧迫、最受关注的环境议题--雾霾.作为一名中学生,下列做法不符合这一主题的是( )
| A. | 选择自行车和公交车作为出行工具 | |
| B. | 让衣服自然晾干,节约用纸,不使用一次性塑料袋 | |
| C. | 将废纸、汽水瓶等收集起来,一次性焚烧 | |
| D. | 拒绝一次性使用一次性木筷,用电子贺卡代替纸制贺卡 |
 化学就在我们身边,从化学的视角认识生活中的有关问题.
化学就在我们身边,从化学的视角认识生活中的有关问题. 如图表示一瓶氧化锌溶液,请用正确的化学用语填空:
如图表示一瓶氧化锌溶液,请用正确的化学用语填空: