题目内容
6.下列实验方案,设计合理的是( )| A. | 证明O2中混有少量CO2-将燃着的木条伸入集气瓶中观察是否熄灭 | |
| B. | 证明CaCl2粉末中混有CaCO3-取样,滴入稀盐酸观察是否有气泡产生 | |
| C. | 除去炭粉中混有的氧化铜-将固体粉末在空气中灼烧 | |
| D. | 除去N2中混有的CO2、CO-将混合气体依次通过澄清的石灰水、灼热的CuO |
分析 A、根据少量的二氧化碳不能出现明显的现象分析;
B、根据碳酸钙和稀盐酸反应产生二氧化碳分析;
C、根据碳粉能够和氧气反应分析;
D、根据除杂的原则分析.
解答 解:A、O2中混有少量CO2-将燃着的木条伸入集气瓶中不能出现明显的现象,故不合理;
B、碳酸钙和稀盐酸反应产生二氧化碳气体,可以证明碳酸钙的存在,故合理;
C、将固体粉末在空气中灼烧,碳粉能够和氧气反应产生二氧化碳,除去的是碳粉而不是氧化铜,故不合理;
D、二氧化碳能够和石灰水反应,氧化铜和一氧化碳反应产生二氧化碳,会增加新的气体,故不合理;
故选项为:B.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
16.以下归纳和总结完全正确的一组是( )
| A.对化学资源的认识 | B.对安全的认识 |
| ①可用塑料来代替部分铜制造汽车零部件 ②稀土是不可再生的重要战略资源,应合理利用和保护 | ①点燃可燃性气体前一定要验纯 ②含有亚硝酸钠的工业用盐可以食用 |
| C.对物质分类的认识 | D.对有机物的认识 |
| ①只含一种元素的物质可能是混合物 ②纯净物一定是由同种分子构成的 | ①有机物不一定都含有碳元素 ②淀粉属于有机高分子化合物 |
| A. | A | B. | B | C. | C | D. | D |
17.在某化学反应A2+3B2=2C中,C物质的化学式符合的是( )
| A. | AB2 | B. | A2B | C. | AB3 | D. | A2B3 |
1.下列变化中,属于物理变化的是( )
| A. | 铁器生锈 | B. | 矿石粉碎 | C. | 食物腐烂 | D. | CO冶铁 |
18.根据常见元素的化合价,下列物质的化学式(括号内)书写错误的是( )
| A. | 氧化镁(MgO) | B. | 氯化铝(AlCl) | C. | 氧化钠(Na2O) | D. | 硫酸亚铁(FeSO4) |
8.物质除杂是化学实验中经常遇到的问题.
【方法探究】为了除去二氧化碳气体中混有的少量一氧化碳,小明设计了三种方案.
上述方案中有两个是合理的,写出合理方案中任意一个反应的化学方程式CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2(或CO2+2NaOH═Na2CO3+H2O、Na2CO3+2HCl═2NaCl+H2O+CO2↑);
【方法提炼】上述两种合理方案体现了物质除杂的不同思路:
思路一:将杂质直接转化为所需物质;
思路二:将所需物质转化为中间物质,在将中间物质转化为所需物质.
【方法运用】
运用思路一:除去氯化镁粉末中混有的少量氯化钡,先加足量的水溶解,再向溶液中加入适量的硫酸镁溶液,过滤、蒸发,即得氯化镁固体.
运用思路二:除去氯化镁粉末中混有的少量氯化钡、氯化钠和硫酸钾.
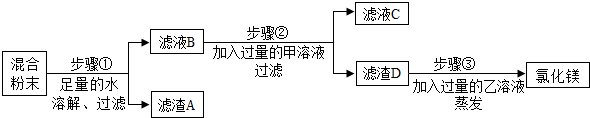
步骤①中反应的化学方程式是BaCl2+K2SO4═BaSO4↓+2KCl,滤液B中一定含有的溶质是氯化钾、氯化钠、氯化镁;
步骤②中反应的化学方程式是2NaOH+MgCl2=Mg(OH)2↓+2NaCl,滤液C中一定含有的阴离子是氯离子和氢氧根离子;
步骤③中乙溶液是HCl(填化学式)溶液.
【方法探究】为了除去二氧化碳气体中混有的少量一氧化碳,小明设计了三种方案.
| 实验方案 | |
| 方案A |  |
| 方案B | 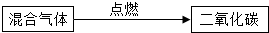 |
| 方案C | 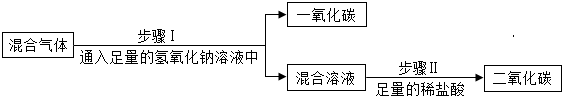 |
【方法提炼】上述两种合理方案体现了物质除杂的不同思路:
思路一:将杂质直接转化为所需物质;
思路二:将所需物质转化为中间物质,在将中间物质转化为所需物质.
【方法运用】
运用思路一:除去氯化镁粉末中混有的少量氯化钡,先加足量的水溶解,再向溶液中加入适量的硫酸镁溶液,过滤、蒸发,即得氯化镁固体.
运用思路二:除去氯化镁粉末中混有的少量氯化钡、氯化钠和硫酸钾.

步骤①中反应的化学方程式是BaCl2+K2SO4═BaSO4↓+2KCl,滤液B中一定含有的溶质是氯化钾、氯化钠、氯化镁;
步骤②中反应的化学方程式是2NaOH+MgCl2=Mg(OH)2↓+2NaCl,滤液C中一定含有的阴离子是氯离子和氢氧根离子;
步骤③中乙溶液是HCl(填化学式)溶液.