题目内容
如表是某同学实验报告的部分内容:
(1)请在表中的空白处补全有关内容;
(2)表中三个反应都是探究 (填物质类别)的化学性质;
(3)实验①和实验②能发生复分解反应的原因是 ;
(4)试举一例说明反应③的实际应用 .
| 实验序号 | 反应物甲 | 反应物乙 | 实验现象 | 化学方程式 |
| ① | 碳酸钠溶液 | 氢氧化钙溶液 | ||
| ② | 碳酸钾溶液 | 氯化钡溶液 | 有白色沉淀产生 | |
| ③ | 碳酸钙 | 稀盐酸 |
(2)表中三个反应都是探究
(3)实验①和实验②能发生复分解反应的原因是
(4)试举一例说明反应③的实际应用
考点:盐的化学性质,复分解反应及其发生的条件,书写化学方程式、文字表达式、电离方程式
专题:常见的盐 化学肥料
分析:(1)根据反应物和反应后生成物书写化学方程式即可
(2)碳酸盐与酸反应能生成气体二氧化碳;碳酸根离子与钙离子、钡离子等金属离子反应能生成沉淀
(3)碳酸根离子与钙离子结合生成了碳酸钙沉淀
(4)反应③是碳酸钙和盐酸反应
(2)碳酸盐与酸反应能生成气体二氧化碳;碳酸根离子与钙离子、钡离子等金属离子反应能生成沉淀
(3)碳酸根离子与钙离子结合生成了碳酸钙沉淀
(4)反应③是碳酸钙和盐酸反应
解答:解:(1)根据反应物和反应后生成物书写化学方程式,碳酸钠与氢氧化钙反应生成氢氧化钠和碳酸钙,有白色沉淀生成,反应的方程式为Na2CO3+Ca(OH)2═2NaOH+CaCO3↓;碳酸钾与氯化钡反应生成碳酸钡和氯化钾,反应的方程式为BaCl2+K2CO3═BaCO3↓+2KCl;
(2)表中三个反应都是探究碳酸盐与酸反应生成气体二氧化碳;碳酸根离子与钙离子反应生成碳酸钙沉淀;
(3)实验①和实验②能发生反应的共同原因是因为碳酸根离子与钙离子结合生成了碳酸钙沉淀;
(4)实验室制取CO2或用盐酸除水垢都是利用此反应原理;
故答案为:(1):①产生白色沉淀;Na2CO3+Ca(OH)2═2NaOH+CaCO3↓;②BaCl2+K2CO3═BaCO3↓+2KCl;③产生白色沉淀;CaCO3+2HCl═CaCl2+H2O+CO2↑
(2)碳酸盐
(3)CO32-与Ca2+反应生成碳酸钙沉淀
(4)实验室制取CO2
(2)表中三个反应都是探究碳酸盐与酸反应生成气体二氧化碳;碳酸根离子与钙离子反应生成碳酸钙沉淀;
(3)实验①和实验②能发生反应的共同原因是因为碳酸根离子与钙离子结合生成了碳酸钙沉淀;
(4)实验室制取CO2或用盐酸除水垢都是利用此反应原理;
故答案为:(1):①产生白色沉淀;Na2CO3+Ca(OH)2═2NaOH+CaCO3↓;②BaCl2+K2CO3═BaCO3↓+2KCl;③产生白色沉淀;CaCO3+2HCl═CaCl2+H2O+CO2↑
(2)碳酸盐
(3)CO32-与Ca2+反应生成碳酸钙沉淀
(4)实验室制取CO2
点评:通过回答本题知道了碳酸根的检验方法,掌握了在分析化学反应后所得物质的成分时不仅考虑生成物有什么,还需要考虑反应物中什么物质发生反应.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
下列燃料中:①煤 ②天然气 ③乙醇 ④一氧化碳,属于较清洁燃料的是( )
| A、①②③ | B、①③④ |
| C、②④ | D、②③ |
关于用红磷燃烧测定空气中氧气含量的实验中,下列说法正确的是( )
| A、燃烧匙中的红磷可以换成蜡烛 |
| B、选用红磷是因为它可以耗尽集气瓶中的氧气,生成固态的五氧化二磷 |
| C、燃烧匙中的红磷越多,水位上升越高 |
| D、本实验可以证明空气中含有氮气、氧气和稀有气体 |
下列符号既能表示一种单质,又能表示一种元素,还能表示一个原子的是( )
| A、N |
| B、S8 |
| C、Al |
| D、O2 |
如图所示实验操作错误的是( )
A、 铁丝在O2中燃烧 |
B、 稀释浓硫酸 |
C、 读取液体体积 |
D、 称量NaCl |
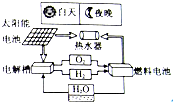 如图是太阳能燃料电池的组成与功能示意图,请据图回答下列问题:
如图是太阳能燃料电池的组成与功能示意图,请据图回答下列问题: