题目内容
16.下列说法合理的是( )| A. | 蓄电池中用到的硫酸溶液是将水加入到浓硫酸中稀释而成 | |
| B. | 糖类和油脂在人体内经氧化放出能量,为维持恒定体温提供能量 | |
| C. | 用石灰石与硫酸铜溶液混合配制防治植物病害的波尔多液 | |
| D. | 农药本身有毒,应该禁止施用农药 |
分析 A、根据稀释浓硫酸的注意事项进行分析;
B、根据糖类和油脂的生理机理来分析;
C、根据波尔多液的成分进行分析;
D、根据禁止施用农药不能保障农业的生产进行分析.
解答 解:A、浓硫酸稀释时,一定要浓硫酸沿器壁慢慢注入水里,并不断用玻璃棒搅拌;切不可将水倒进浓硫酸里;故A说法错误;
B、糖类和油脂在人体内经氧化放出能量,为机体活动和维持恒定体温提供能量;故B说法正确;
C、石灰石是碳酸钙,氢氧化钙能与硫酸铜混合配制波尔多液;故C说法错误;
D、农药本身有毒,应该合理施用农药,不能禁止施用,故D说法错误;
故选:B.
点评 化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关的化学知识也是重要的中考热点之一.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.化学与生活密切相关,下列做法错误的是( )
| A. | 油锅的油不慎着火,可用锅盖盖灭 | |
| B. | 废旧电池埋入土中对环境不会产生不良影响 | |
| C. | 为缓解温室效应,应倡导“低碳生活” | |
| D. | 煤脱硫、利用清洁能源是预防 酸雨的有效措施 |
4.实验小组的同学设计了探究铁、铜、银三种金属的活动性顺序方案.其中所选试剂组合正确的是( )
| A. | 硫酸亚铁溶液、铜、银 | B. | 硫酸亚铁溶液、铜、硝酸银溶液 | ||
| C. | 硫酸亚铁溶液、硫酸铜溶液、银 | D. | 稀硫酸、铁、铜、银 |
11.下列关于空气的说法中正确的是( )
| A. | 空气污染指数50-100,说明空气质量状况为优 | |
| B. | 空气中氮气体积分数约为21% | |
| C. | 空气中含量较多且化学性质不活泼的是氮气 | |
| D. | 洁净的空气是纯净物 |
1.把足量锌粒加入装有盐酸的试管中,发现随着反应的进行,产生气体的速度逐渐加快,一段时间后逐渐减慢,最后停止产生气体.在反应过程中,溶液的温度也先随之升高,最后下降到室温.于是,同学们设计实验来探究“一定质量的锌粒和同体积盐酸反应快慢的影响因素”.测得实验数据如下:
一定质量的锌粒与同体积盐酸溶液反应实验数据表
(1)锌粒和盐酸反应的化学化学方程式为Zn+2HCl═ZnCl2+H2↑.
(2)分析实验数据得出:一定质量的锌粒和同体积盐酸反应,影响锌和酸反应快慢的主要因素有盐酸溶液浓度、反应时溶液温度.
(3)可以通过比较反应开始到2分钟产生的气体体积(或相同时间内产生的气体体积)实验数据来确定锌和酸反应的快慢.
(4)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快原因金属锌和盐酸反应放出热量,加快反应速率.
一定质量的锌粒与同体积盐酸溶液反应实验数据表
| 盐酸溶液 浓度 | 反应开始时酸溶液的 温度 | 反应开始到2分钟产生的 气体体积 | 反应结束共产生 气体体积 |
| 5% | 20℃ | 10mL | 60mL |
| 10% | 20℃ | 19mL | 118mL |
| 15% | 20℃ | 28mL | 175mL |
| 5% | 35℃ | 28mL | 60mL |
| 10% | 35℃ | 72mL | 118mL |
| 15% | 35℃ | 103mL | 175mL |
(2)分析实验数据得出:一定质量的锌粒和同体积盐酸反应,影响锌和酸反应快慢的主要因素有盐酸溶液浓度、反应时溶液温度.
(3)可以通过比较反应开始到2分钟产生的气体体积(或相同时间内产生的气体体积)实验数据来确定锌和酸反应的快慢.
(4)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快原因金属锌和盐酸反应放出热量,加快反应速率.
5.下列关于“物质--用途--性质”的说法不正确的是( )
| A. | 汽油--去除油污--能乳化油污 | |
| B. | 天然气--用作燃料--具有可燃性 | |
| C. | 液氮--用作冷冻麻醉剂--能气化吸热 | |
| D. | 氢氧化镁--治疗胃酸过多症--能与胃液中的盐酸发生中和反应 |
15.下列实验操作图示正确的是( )
| A. | 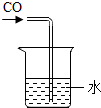 处理尾气 | B. |  盛放二氧化碳 | C. | 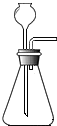 实验室制取CO2 | D. | 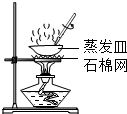 蒸发食盐水 |
