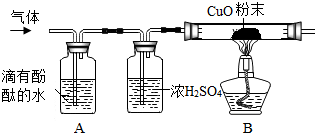
题目内容
17.白色粉笔是一种常用的教学用品,已知某品牌白色粉笔的主要成分中含有钙元素,并属于碱、盐中的一种物质.某化学兴趣小组的同学一起探究该粉笔的组成.【提出问题】
白色粉笔的主要成分是什么?
【作出猜想】
①碳酸钙;②硫酸钙;③硝酸钙.
【查阅资料】
硝酸钙易溶于水;硫酸钙微溶于水;硫酸钡不溶于水,也不溶于稀硝酸.
【实验探究】
(1)小军取一段白色粉笔(约1g),在研钵中研成粉末,倒入大烧杯中,加入100毫升蒸馏水,充分搅拌,静置,发现烧杯底部有较多的白色固体未溶解.说明猜想③不成立;
(2)小军将烧杯中的物质过滤,然后取少量滤渣于试管中,并滴加稀盐酸,看到的现象为无气泡产生,证明猜想①不成立;
(3)小兵取少量滤液于试管中,滴加Ba(NO3)2溶液和稀硝酸,有白色不溶物产生,发生反应的化学方程式为CaSO4+Ba(NO3)2=Ca(NO3)2+BaSO4↓;
【实验结论】
根据上述探究中的实验现象,请你写出该粉笔主要成分的化学式为CaSO4;
【继续探究】
为防止小兵的实验废液污染环境,小天对其反应后的滤液进行探究,请你帮助他完成实验报告:
| 实 验 操 作 | 实 验 现 象 | 实 验 结 论 |
| 取样,滴加氯化钡溶液 | 产生白色沉淀 | 滤液中含有硝酸钡 |
分析 【实验探究】(1)根据硝酸钙易溶于水进行解答;
(2)根据碳酸钙和盐酸反应会生成二氧化碳气体进行解答;
(3)根据硫酸钙和硝酸钡溶液反应生成硫酸钡沉淀和硝酸钙,且硫酸钡不溶于水稀硝酸进行解答;
【实验结论】根据实验探究可知该粉笔主要成分硫酸钙进行解答;
【继续探究】根据硫酸钙和硝酸钡溶液反应生成硫酸钡沉淀和硝酸钙,滴加Ba(NO3)2溶液和稀硝酸后溶液中一定含有硝酸钙和稀硝酸,不知道是否含有硫酸钙进行解答.
解答 解:【实验探究】(1)硝酸钙易溶于水,所以取一段白色粉笔(约1g),在研钵中研成粉末,倒入大烧杯中,加入100毫升蒸馏水,充分搅拌,静置,发现烧杯底部有较多的白色固体未溶解.说明猜想③不成立;故填:③;
(2)碳酸钙和盐酸反应会生成二氧化碳气体,所以将烧杯中的物质过滤,然后取少量滤渣于试管中,并滴加稀盐酸,看到无气泡产生的现象,证明猜想①不成立;故填:无气泡产生;
(3)硫酸钙和硝酸钡溶液反应生成硫酸钡沉淀和硝酸钙,且硫酸钡不溶于水稀硝酸,所以兵取少量滤液于试管中,滴加Ba(NO3)2溶液和稀硝酸,有白色不溶物产生,说明主要成分是硫酸钙,发生反应的化学方程式为CaSO4+Ba(NO3)2=Ca(NO3)2+BaSO4↓;故填:CaSO4+Ba(NO3)2=Ca(NO3)2+BaSO4↓;
【实验结论】硫酸钙和硝酸钡溶液反应生成硫酸钡沉淀和硝酸钙,且硫酸钡不溶于水稀硝酸,所以兵取少量滤液于试管中,滴加Ba(NO3)2溶液和稀硝酸,有白色不溶物产生,说明主要成分是硫酸钙;故填:CaSO4;
【继续探究】硫酸钙和硝酸钡溶液反应生成硫酸钡沉淀和硝酸钙,滴加Ba(NO3)2溶液和稀硝酸后溶液中一定含有硝酸钙和稀硝酸,不知道是否含有硫酸钙,所以试验方案:
| 实 验 操 作 | 实 验 现 象 | 实 验 结 论 |
| 取样,滴加氯化钡溶液 | 产生白色沉淀 | 滤液中含有硝酸钡 |
【实验探究】
(1)③;
(2)无气泡产生;
(3)CaSO4+Ba(NO3)2=Ca(NO3)2+BaSO4↓;
【实验结论】CaSO4;
【继续探究】
| 实 验 操 作 | 实 验 现 象 | 实 验 结 论 |
| 取样,滴加氯化钡溶液 | 产生白色沉淀 | 滤液中含有硝酸钡 |
点评 本题考查了常见物质成分的推断,完成此题,可以依据物质的性质进行.

 某无色的溶液中含有的离子如图所示,其中X可能是( )
某无色的溶液中含有的离子如图所示,其中X可能是( )| A. | Cu2+ | B. | CO32- | C. | OH- | D. | Ag+ |
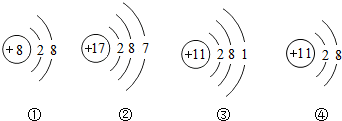
| A. | ①④的化学性质比较稳定 | B. | ③④属于同种元素 | ||
| C. | ②容易得到电子 | D. | ④是一种阴离子 |

| A. | ①②③ | B. | ①③⑤ | C. | ①④⑤ | D. | ③④⑤ |
| A. | 澄清的生理盐水是纯净物 | B. | 合金属于复合材料 | ||
| C. | 磷酸二氢铵属于复合肥料 | D. | 氯化钠固体是导体 |