题目内容
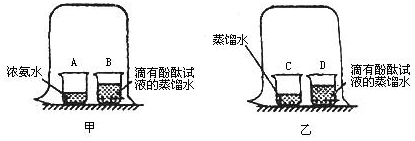
5.现有一包白色粉末,其中含有CuSO4、BaCl2、NaOH、Na2CO3中的一种或几种,某化学小组为确定白色粉末的成分,进行了如下实验:(Ⅰ)取一定量白色粉末,加入足量水,振荡,得到无色透明溶液;(Ⅱ)取少量(Ⅰ)的溶液,加入足量盐酸,有气泡产生.(提示:BaCO3难溶于水;Na2CO3的水溶液呈碱性)(1)该白色粉末中肯定含有的物质是:碳酸钠;可能含有的物质是氢氧化钠.
(2为确定可能含有的物质是否存在,还需做什么实验?请写出简要的实验步骤:加入足量的氯化钙溶液除去碳酸钠,然后加入酚酞试液,观察酚酞试液是否变红.
(3)写出往(Ⅰ)中所得溶液加入足量盐酸时,所发生反应的化学方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
分析 根据题干提供的信息进行分析解答,(Ⅰ)取一定量白色粉末,加入足量水,振荡,得到无色透明溶液,由于硫酸铜溶液是蓝色的,故一定不含有硫酸铜,由于氯化钡能与碳酸钠反应产生碳酸钡沉淀,故氯化钡和碳酸钠不能同时存在;(Ⅱ)取少量(Ⅰ)的溶液,加入足量盐酸,有气泡产生,说明一定含有碳酸钠,故氯化钡不含有,不能确定是否含有氢氧化钠,据此解答.
解答 解:(Ⅰ)取一定量白色粉末,加入足量水,振荡,得到无色透明溶液,由于硫酸铜溶液是蓝色的,故一定不含有硫酸铜,由于氯化钡能与碳酸钠反应产生碳酸钡沉淀,故氯化钡和碳酸钠不能同时存在;(Ⅱ)取少量(Ⅰ)的溶液,加入足量盐酸,有气泡产生,说明一定含有碳酸钠,故氯化钡不含有,不能确定是否含有氢氧化钠;
(1)一定存在碳酸钠,可能存在氢氧化钠,故填:碳酸钠;氢氧化钠;
(2)要确定氢氧化钠的存在,首先需要加入足量的氯化钙溶液除去碳酸钠,然后加入酚酞试液,观察酚酞试液是否变红,故填:加入足量的氯化钙溶液除去碳酸钠,然后加入酚酞试液,观察酚酞试液是否变红;
(3)加入盐酸产生气泡是因为碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,故填:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
点评 本题考查的是物质的成分的推断,完成此题,可以依据已有的物质的性质进行.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.实验操作错误的是( )
| A. |  倾倒液体 | B. | 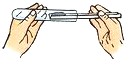 装入固体粉末 | C. | 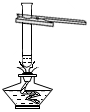 加热液体 | D. | 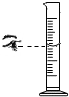 读取液体体积 |
15.下列变化都属化学变化的是( )
| A. | 铁丝弯曲,灯泡通电发光 | B. | 高粱酿成酒,洗净的铁锅出现锈迹 | ||
| C. | 瓷碗破碎,大米久置发霉 | D. | 纸张燃烧,石蜡熔化 |