题目内容
6.台湾“毒淀粉”是在淀粉中添加了对人体有害的马来酸(C4H4O4),长期超标食用“毒淀粉”,将极大损伤肾脏功能.下列有关马来酸的叙述正确的是( )| A. | 马来酸属于氧化物 | B. | 马来酸由12个原子构成 | ||
| C. | 马来酸由三种元素组成 | D. | 马来酸中碳元素的质量分数最大 |
分析 A.根据氧化物的概念来分析;
B.根据化合物化学式的意义来分析;
C.根据物质的组成来分析;
D.根据化合物中元素质量分数大小的比较方法来分析.
解答 解:A.氧化物中只含有两种元素,而马来酸中含有三种元素,不属于氧化物,故错误;
B.马来酸是由分子构成的而不是由原子直接构成的,故错误;
C.马来酸是由碳、氢、氧三种元素组成的,故正确;
D.马来酸中,碳、氢、氧三种元素的质量比为(12×4):(1×4):(16×4)=12:1:16,可见其中氧元素的质量分数最大,故错误.
故选C.
点评 本题难度不大,掌握化学式的有关计算、氧化物的特征并能灵活运用是正确解答本题的关键.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
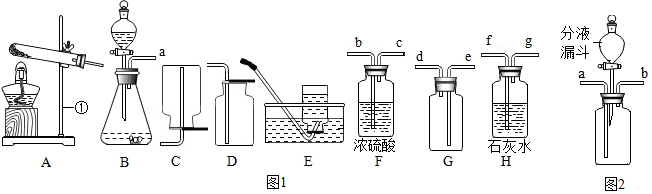
8. 如图为验证水的组成的实验装置,下列有关说法正确的是( )
如图为验证水的组成的实验装置,下列有关说法正确的是( )
 如图为验证水的组成的实验装置,下列有关说法正确的是( )
如图为验证水的组成的实验装置,下列有关说法正确的是( )| A. | 正极和负极产生的气体质量比为1:2 | |
| B. | 正极产生的气体能使带火星的木条复燃 | |
| C. | 每个水分子由两个氢原子和一个氧原子构成 | |
| D. | 水是由一个氧原子和氢原子组成的 |
14.下列说法错误的是( )
| A. | 分离液态空气法制氧气属于分解反应 | |
| B. | 电解水生成氢气和氧气,说明水是由氢、氧两种元素组成的 | |
| C. | 自然界的水多数是混合物,通过蒸馏方法可得到纯净物 | |
| D. | 打开盛浓盐酸的瓶盖,可观察到瓶口有白雾出现 |
11.某班同学用氢氧化钠溶液和稀盐酸进行中和反应实验.
(1)甲同学实验操作如图甲.
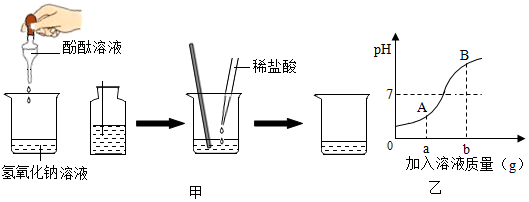
在烧杯中加入约5mL氢氧化钠溶液,滴入几滴无色酚酞溶液,此时溶液呈红色.使用胶头滴管吸取液体时,要先按着橡胶帽排干净空气,再放入滴瓶中吸取液体.
接着用滴管滴入一定量的稀盐酸,再用玻璃棒搅拌,发现溶液为无色,于是甲同学得出两者恰好中和的结论,反应的化学方程式为NaOH+HCl═NaCl+H2O.
(2)乙同学对甲同学的结论提出了质疑,并对反应后溶液中的溶质成分进行探究.
【实验探究】
反应后溶液中的溶质是什么?
猜想一:只有NaCl. 猜想二:NaCl和HCl.猜想三:NaCl和NaOH.
以上猜想中,你觉得不合理的是猜想三.
为了验证另外两种猜想,乙同学设计如下实验方案:
(3)图乙是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是CD(多选)
A.该反应是稀HCl滴入NaOH溶液中
B.ag是指加入氢氧化钠固体质量
C.A点溶液的溶质为HCl和NaCl
D.检验B点溶液的溶质先滴加足量的Mg(NO3)2,静置后再滴入少量AgNO3.
(1)甲同学实验操作如图甲.

在烧杯中加入约5mL氢氧化钠溶液,滴入几滴无色酚酞溶液,此时溶液呈红色.使用胶头滴管吸取液体时,要先按着橡胶帽排干净空气,再放入滴瓶中吸取液体.
接着用滴管滴入一定量的稀盐酸,再用玻璃棒搅拌,发现溶液为无色,于是甲同学得出两者恰好中和的结论,反应的化学方程式为NaOH+HCl═NaCl+H2O.
(2)乙同学对甲同学的结论提出了质疑,并对反应后溶液中的溶质成分进行探究.
【实验探究】
反应后溶液中的溶质是什么?
猜想一:只有NaCl. 猜想二:NaCl和HCl.猜想三:NaCl和NaOH.
以上猜想中,你觉得不合理的是猜想三.
为了验证另外两种猜想,乙同学设计如下实验方案:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量反应后的溶液于试管中滴入Na2CO3溶液 | 产生气泡 | 猜想二成立 |
| 取少量反应后的溶液于试管中加入锌粒 | 没有气泡产生 | 猜想一成立 |
A.该反应是稀HCl滴入NaOH溶液中
B.ag是指加入氢氧化钠固体质量
C.A点溶液的溶质为HCl和NaCl
D.检验B点溶液的溶质先滴加足量的Mg(NO3)2,静置后再滴入少量AgNO3.
15.下列物质的水溶液能使紫色石蕊溶液变红色的是( )
| A. | NaCl | B. | NH3 | C. | H2SO4 | D. | NaOH |
16.某同学在实验室进行有关浓硫酸的实验,观察到瓶上的标签如下表所示,用于配制稀硫酸.求:欲配制1000克质量分数为19.6%的稀硫酸,
(1)需要多少克这种浓硫酸?
(2)需要加入多少毫升水?
| 浓硫酸(H2SO4)500毫升 | |
| 溶质的质量分数 | 98% |
| 密度 | 1.84克/厘米3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封储藏 | |
(2)需要加入多少毫升水?