题目内容
8.味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”.请回答下列问题:(1)称取5.0g味精配制成50g溶液,量取蒸馏水的量筒规格是B.(填字母)
A.10mL B.50mL C.100mL
(2)如图是配制过程,正确的操作顺序为②①④③.(填序号)

(3)在其他操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液的谷氨酸钠质量分数偏小(填“偏大”、“偏小”或“无影响”).
分析 (1)利用溶剂质量=溶液质量-溶质质量,计算出所需水的质量,由所需水的体积判断所需量筒的量程.
(2)根据配制溶质质量分数一定的溶液的基本步骤进行分析解答.
(3)用量筒量取水时,仰视液面,读数比实际液体体积小,会造成实际量取的水的体积偏大,进行分析解答.
解答 解:(1)溶溶剂质量=溶液质量-溶质质量,则所需蒸馏水的质量=50g-5.0g=45.0g(合45.0mL),应选用50mL的量筒.
(2)配制溶质质量分数一定的溶液,首先计算配制溶液所需谷氨酸钠和水的质量,再称量所需的谷氨酸钠和量取水,最后进行溶解,故正确的操作顺序为②①④③.
(3)在其他操作均正确的情况下,用量筒量取水时,仰视液面,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数偏小.
故答案为:(1)B;(2)②①④③;(3)偏小.
点评 本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤、注意事项等是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.某校兴趣小组的同学在实验室中完成制取氧气的实验,他们取80g过氧化氢溶液和5g二氧化锰混合放入锥形瓶中,并在不同时刻测定锥形瓶内剩余物体的质量,如表:
根据表中数据,完成下列问题:
(1)完全反应时生成氧气的质量是6.4g.
(2)过氧化氢溶液中过氧化氢的质量是多少克?
| 反应时间/min | T1 | T2 | T3 | T4 | T5 |
| 剩余物质/g | 80.0 | 79.2 | 78.8 | 78.6 | 78.6 |
(1)完全反应时生成氧气的质量是6.4g.
(2)过氧化氢溶液中过氧化氢的质量是多少克?
16.有一包不纯的K2CO3粉末,可能含有Na2CO3、BaSO4、CuCl2、KCl、KNO3、Ca(NO3)2中的一种或几种,为分析含有的杂质,现进行如下实验.
(1)取样溶于水,无固体残留,得无色溶液.
(2)取上述溶液适量,滴加AgNO3溶液,有白色沉淀,再加入足量稀HNO3,沉淀部分溶解.
(3)为确定Na2CO3是否存在,某同学称取13.8g粉末溶于水,加入足量BaCl2溶液,充分反应生成19.7g沉淀质量.
下列判断正确的是( )
(1)取样溶于水,无固体残留,得无色溶液.
(2)取上述溶液适量,滴加AgNO3溶液,有白色沉淀,再加入足量稀HNO3,沉淀部分溶解.
(3)为确定Na2CO3是否存在,某同学称取13.8g粉末溶于水,加入足量BaCl2溶液,充分反应生成19.7g沉淀质量.
下列判断正确的是( )
| A. | 粉末中一定不含有BaSO4、CuCl2 KNO3 | |
| B. | 粉末中一定含有KCl、KNO3、Ca(NO3)2 | |
| C. | 粉末中一定含有Na2CO3 | |
| D. | 该粉末由K2CO3、Na2CO3、KCl、KNO3、Ca(NO3)2组成 |
13.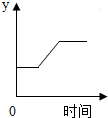 一定质量的高锰酸钾受热分解,某些量随时间变化的情况如图所示,横坐标表示受热的时间,根据图象判断,纵坐标可能表示( )
一定质量的高锰酸钾受热分解,某些量随时间变化的情况如图所示,横坐标表示受热的时间,根据图象判断,纵坐标可能表示( )
 一定质量的高锰酸钾受热分解,某些量随时间变化的情况如图所示,横坐标表示受热的时间,根据图象判断,纵坐标可能表示( )
一定质量的高锰酸钾受热分解,某些量随时间变化的情况如图所示,横坐标表示受热的时间,根据图象判断,纵坐标可能表示( )| A. | 固体中氧元素的质量 | B. | 生成氧气的质量 | ||
| C. | 固体中钾元素的质量分数 | D. | 固体中锰元素的质量 |
20.化学影响着社会的发展和人们的生活质量.以下分析不正确的是( )
| A. | 甲醛水溶液浸泡过的鱼,食用后不会危害人体健康 | |
| B. | 利用锂电池给数码相机供电 | |
| C. | 糖类和油脂都可以为人体提供能量 | |
| D. | 鸡蛋是富含蛋白质的食品 |
17.规范实验操作是获得实验成功的重要保证.下列实验操作正确的是( )
| A. |  闻气体气味 | B. |  取用块状固体 | C. | 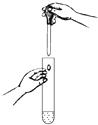 滴加液体 | D. | 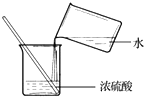 稀释浓硫酸 稀释浓硫酸 |