题目内容
3.下列实验中,能达到相应目的是( )| A. | 分离CaCO3和CaCl2固体:取样,加足量水溶解,过滤 | |
| B. | 制备Fe(OH)3:将Fe2(SO4)3溶液和适量的Ba(OH)2溶液混合,过滤 | |
| C. | 除去CO2中的HCl气体和水蒸气:将混合气体一次通过浓硫酸、NaOH溶液 | |
| D. | 鉴别稀盐酸、NaOH和NaCl三种溶液:取样,分别滴入酚酞溶液后再相互混合 |
分析 A、根据碳酸钙难溶于水进行分析;
B、根据硫酸铁和氢氧化钡会生成氢氧化铁沉淀和硫酸钡沉淀进行分析;
C、根据气体通过氢氧化钠溶液也会携带水蒸气进行分析;
D、根据酚酞在酸、碱、盐中显示不同的颜色进行分析.
解答 解:A、碳酸钙难溶于水,分离CaCO3和CaCl2固体:不用取样,直接加足量水溶解,过滤,蒸发,故A错误;
B、硫酸铁和氢氧化钡会生成氢氧化铁沉淀和硫酸钡沉淀,过滤后的沉淀是硫酸钡沉淀和氢氧化铁沉淀的混合物,故B错误;
C、气体通过氢氧化钠溶液也会携带水蒸气,故C错误;
D、取样品,加入酚酞,溶液显红色的是氢氧化钠、不变色的是氯化钠、盐酸,在变红色的氢氧化钠溶液中,滴入剩余的两种溶液,颜色褪去的是盐酸,剩下的是氯化钠,可以鉴别,故D正确.
故选:D.
点评 本题是有关实验方案的设计和评价的考查,要求学生熟悉所实验的内容及原理,完成此题,可以依据已有的知识进行.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
18.下列说法中,错误的是( )
| A. | 酒精是一种可再生能源 | B. | 在加油站内应严禁烟火 | ||
| C. | 二氧化碳是一种空气污染物 | D. | 金属的回收利用可节约金属资源 |
15.下列属于化学变化的是( )
| A. | 石蜡熔化 | B. | 酒精挥发 | C. | 胆矾研碎 | D. | 粮食酿酒 |
12.某学习小组探究氢氧化钙溶液的化学性质,并作了延伸探究.
探究一:甲同学设计了如下实验方案,请你帮助完成实验报告.
【提出问题】实验方案(3)褪色后溶液中的溶质是什么?
【查阅资料】CaCl2溶液呈中性.
【作出猜想】乙同学从反应情况分析,溶液中除含少量酚酞外,溶质可能有以下三种情况:
①CaCl2;②CaCl2和HCl;③CaCl2和Ca(OH)2
【分析讨论】丙同学从实验现象分析得出:猜想③肯定不合理,其理由是稀盐酸加入滴有酚酞的石灰水中,红色褪为无色,说明溶液为中性或酸性,不可能有氢氧化钙.
探究二:
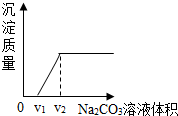
丁同学为进一步验证乙同学的猜想,设计实验如下:将实验方案(3)褪色后溶液倒入烧杯中,向其中逐滴滴加稀碳酸钠溶液至过量,边滴边振荡.实验后得出产生沉淀质量与滴加碳酸钠溶液体积之间的关系,如图所示.写出实验过程中的现象滴加碳酸钠溶液,开始先产生气泡,随后才产生沉淀,溶液最终变红色.
【得出结论】乙同学的猜想中,②(填序号)合理.
【反思讨论】
学习小组结合图象,分析了丁同学实验过程中烧杯内溶液的变化.下列说法正确的是AB.(填序号)
A.溶液质量逐渐增大 B.氯化钠质量逐渐增大,V2后不变
C.氯化钙的质量先增大后减小 D.溶液的pH一直在增大.
探究一:甲同学设计了如下实验方案,请你帮助完成实验报告.
| 方案 | (1) | (2) | (3) |
| 实验操作 | 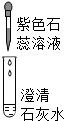 | 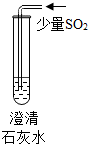 |  |
| 现象 | 溶液变为蓝色 | 澄清石灰水变浑浊 | 红色褪为无色 |
| 结论或解释 | 氢氧化钙溶液能使石蕊等酸碱指示剂变色 | 氢氧化钙溶液能与某些非金属氧化物反应生成盐和水.二氧化硫与澄清石灰水反应的化学方程式是 SO2+Ca(OH)2═CaSO3↓+H2O | 氢氧化钙溶液能与酸发生中和反应 |
【查阅资料】CaCl2溶液呈中性.
【作出猜想】乙同学从反应情况分析,溶液中除含少量酚酞外,溶质可能有以下三种情况:
①CaCl2;②CaCl2和HCl;③CaCl2和Ca(OH)2
【分析讨论】丙同学从实验现象分析得出:猜想③肯定不合理,其理由是稀盐酸加入滴有酚酞的石灰水中,红色褪为无色,说明溶液为中性或酸性,不可能有氢氧化钙.
探究二:
丁同学为进一步验证乙同学的猜想,设计实验如下:将实验方案(3)褪色后溶液倒入烧杯中,向其中逐滴滴加稀碳酸钠溶液至过量,边滴边振荡.实验后得出产生沉淀质量与滴加碳酸钠溶液体积之间的关系,如图所示.写出实验过程中的现象滴加碳酸钠溶液,开始先产生气泡,随后才产生沉淀,溶液最终变红色.

【得出结论】乙同学的猜想中,②(填序号)合理.
【反思讨论】
学习小组结合图象,分析了丁同学实验过程中烧杯内溶液的变化.下列说法正确的是AB.(填序号)
A.溶液质量逐渐增大 B.氯化钠质量逐渐增大,V2后不变
C.氯化钙的质量先增大后减小 D.溶液的pH一直在增大.
13.下列物质,属于纯净物的是( )
| A. | 陈醋 | B. | 矿泉水 | C. | 苹果汁 | D. | 水蒸气 |
 根据如图所示某牙膏商标上的部分文字,用化学用语填空:
根据如图所示某牙膏商标上的部分文字,用化学用语填空: