题目内容
13.等质量的质量分数均为4%的氢氧化钠溶液与稀盐酸充分反应,所得溶液呈( )| A. | 碱性 | B. | 酸性 | C. | 中性 | D. | 无法判断 |
分析 根据氢氧化钠与稀盐酸反应的化学方程式,判断完全反应后剩余的是哪一种溶液,进行分析判断.
解答 解:等质量的质量分数均为4%的氢氧化钠溶液与稀盐酸充分反应,盐酸与氢氧化钠溶液所含溶质的质量相等.
反应中消耗盐酸与氢氧化钠的质量比关系如下:
HCl+NaOH═NaCl+H2O
36.5 40
可知36.5份质量的盐酸与40份质量的氢氧化钠恰好完全反应,则等质量的质量分数均为4%的氢氧化钠溶液与稀盐酸充分反应,稀盐酸有剩余,溶液显酸性.
故选:B.
点评 本题难度不大,掌握中和反应应用,根据化学方程式的计算判断出反应后剩余的物质是正确解答本题的关键.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
1.某花圃的花卉缺乏磷元素,应施用的化肥是( )
| A. | K2CO3 | B. | KNO3 | C. | CO(NH2)2 | D. | Ca(H2PO4)2 |
18.KNO3能使作物枝叶繁茂,又能使其茎秆粗壮、增强抗倒伏能力.它属于( )
| A. | 氮肥 | B. | 磷肥 | C. | 钾肥 | D. | 复合肥料 |
5.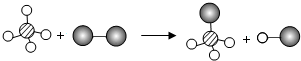 某化学反应的微现示意图如图所示(不同小球代表不同的原子).关于该图说法下列错误的是( )
某化学反应的微现示意图如图所示(不同小球代表不同的原子).关于该图说法下列错误的是( )
 某化学反应的微现示意图如图所示(不同小球代表不同的原子).关于该图说法下列错误的是( )
某化学反应的微现示意图如图所示(不同小球代表不同的原子).关于该图说法下列错误的是( )| A. | 反应前后共有四种分子 | B. | 反应前后分子没有变化 | ||
| C. | 反应前后原子没有变化 | D. | 反应前后原子的组合方式发生变化 |
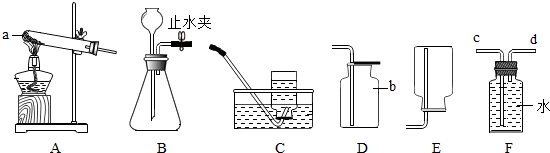
 晚上,静静和妈妈一起做晚饭.
晚上,静静和妈妈一起做晚饭.
 我国化工专家侯德榜发明了侯氏制碱法,为世界制碱工业作出了突出贡献.
我国化工专家侯德榜发明了侯氏制碱法,为世界制碱工业作出了突出贡献.