题目内容
在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量关系,能用如图曲线表示的是( )
序号 | 甲 | 乙 |
① | HNO3溶液 | NaOH溶液 |
② | HCl溶液 | 石灰石粉末 |
③ | CaCl2溶液 | Na2CO3溶液 |
④ | H2SO4溶液 | 锌粒 |
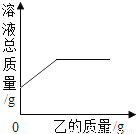
A. ①② B. ②④ C. ②③④ D. ①②④
 B
【解析】
①HNO3溶液中加入NaOH溶液会发生中和反应,不管反应是否停止溶液总质量应该是随着乙的加入而不断上升的,图象上不会有水平的那个阶段;②开始时,溶液总质量就是盐酸的质量,随着加入石灰石粉末,生成氯化钙与二氧化碳及水,溶液质量是不断增加的,当大理石和盐酸全部反应完时,溶液质量就不变了;③氯化钙溶液与碳酸钠反应时会生成碳酸钙沉淀,所以溶液质量应该先减小,直到反应结束后总溶液的...
B
【解析】
①HNO3溶液中加入NaOH溶液会发生中和反应,不管反应是否停止溶液总质量应该是随着乙的加入而不断上升的,图象上不会有水平的那个阶段;②开始时,溶液总质量就是盐酸的质量,随着加入石灰石粉末,生成氯化钙与二氧化碳及水,溶液质量是不断增加的,当大理石和盐酸全部反应完时,溶液质量就不变了;③氯化钙溶液与碳酸钠反应时会生成碳酸钙沉淀,所以溶液质量应该先减小,直到反应结束后总溶液的...
除去下列物质中的少量杂质(括号内的物质),所选用的试剂及操作方法均正确的是( )
选项 | 物质 | 所用试剂 | 操作方法 |
A | CO2(HCl) | 过量氢氧化钠溶液 | 洗气 |
B | NaCl(NaOH) | 适量稀盐酸 | 蒸发结晶 |
C | KCl(MnO2) | 足量蒸馏水 | 溶解、过滤、洗涤、干燥 |
D | 稀盐酸(稀硫酸) | 适量硝酸钡溶液 | 过滤 |
A. A B. B C. C D. D
 B
【解析】
原料二氧化碳会和氢氧化钠反应,A选项错误;除去氯化钠中的氢氧化钠加入盐酸可以反应掉氢氧化钠,而不引入心的杂质,B选项正确;将氯化钾和二氧化锰的混合物加水过滤后,氯化钾在滤液中,操作应该是:溶解、过滤、蒸发结晶、烘干,C选项错误;除去稀盐酸中的稀硫酸加入硝酸钡会引入新的杂质,应该加入氯化钡,D选项错误;故选择B项。
B
【解析】
原料二氧化碳会和氢氧化钠反应,A选项错误;除去氯化钠中的氢氧化钠加入盐酸可以反应掉氢氧化钠,而不引入心的杂质,B选项正确;将氯化钾和二氧化锰的混合物加水过滤后,氯化钾在滤液中,操作应该是:溶解、过滤、蒸发结晶、烘干,C选项错误;除去稀盐酸中的稀硫酸加入硝酸钡会引入新的杂质,应该加入氯化钡,D选项错误;故选择B项。 学习了工业上分离液态空气制取氧气的方法之后,某学习小组在探究“从空气中制取氮气”时,提出了以下实验方案,并设计了如下实验装置图:(假设每步反应都能把气体充分除去)
空气 氮气和氧气
氮气和氧气  氮气
氮气
步骤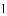
 、
、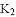 、
、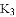 ,通入空气,利用装置
,通入空气,利用装置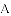
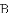
步骤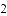
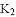 、
、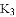 ,用凸透镜聚光,引燃白磷使其燃烧,以去除瓶内氧气.请回答如下问题:
,用凸透镜聚光,引燃白磷使其燃烧,以去除瓶内氧气.请回答如下问题:

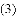
①白磷不足②装置漏气③步骤
A.①②③ B.①③④ C.②③④ D.①②③④
 氮气氢氧化钠溶液浓硫酸D氮气中还含有稀有气体和其它杂质
【解析】
(1)根据氮气与氧气的沸点分析;(2)根据题意“利用装置和,去除水蒸气和二氧化碳”分析;(3)根据氮气不纯分析;(5)根据稀有气体没有除去分析。
(1)工业上制取氧气时,除去空气中的水蒸气和二氧化碳之后,通过控制温度将沸点较低的氮气先蒸腾出来;
(2)氢氧化钠溶液用于吸收二氧化碳,A装置内所装试剂是氢氧化钠溶...
氮气氢氧化钠溶液浓硫酸D氮气中还含有稀有气体和其它杂质
【解析】
(1)根据氮气与氧气的沸点分析;(2)根据题意“利用装置和,去除水蒸气和二氧化碳”分析;(3)根据氮气不纯分析;(5)根据稀有气体没有除去分析。
(1)工业上制取氧气时,除去空气中的水蒸气和二氧化碳之后,通过控制温度将沸点较低的氮气先蒸腾出来;
(2)氢氧化钠溶液用于吸收二氧化碳,A装置内所装试剂是氢氧化钠溶... 在一烧杯中盛有42.2gCaCO3和CaCl2的粉末状混合物,向其中264.6g水,使混合物中的可溶物完全溶解。然后再向其中逐滴加如溶质的质量分数为10%的稀盐酸,烧杯中难溶固体物质的质量与所滴入稀盐酸的质量关系曲线如图所示。请根据题意回答下列问题:

⑴在滴入稀盐酸的过程中,观察到的明显现象是:
①_______________________
②_______________________
⑵当滴入10%的稀盐酸至图中A点时,烧杯中溶液里含有的溶质是(写化学式)______________。
⑶当滴入10%的稀盐酸146g时(即B点),试通过计算,求此时烧杯中所得不饱和溶液的溶质质量分数。______________
 固体物质不断溶解 有气体产生(或有气泡冒出) CaCl2 10%
【解析】 (1).碳酸钙固体与稀盐酸反应有气体产生。⑵CaCO3+2HCl=CaCl2+H2O+CO2↑,当滴入10%的稀盐酸至图中A点时,稀盐酸不足,烧杯中溶液里含有的溶质是CaCl2 ,⑶当滴入10%的稀盐酸146g时(即B点),碳酸钙与稀盐酸恰好反应,设反应掉的碳酸钙的质量为x,生成氯化钙的质量为y,生成二氧化碳的质量为...
固体物质不断溶解 有气体产生(或有气泡冒出) CaCl2 10%
【解析】 (1).碳酸钙固体与稀盐酸反应有气体产生。⑵CaCO3+2HCl=CaCl2+H2O+CO2↑,当滴入10%的稀盐酸至图中A点时,稀盐酸不足,烧杯中溶液里含有的溶质是CaCl2 ,⑶当滴入10%的稀盐酸146g时(即B点),碳酸钙与稀盐酸恰好反应,设反应掉的碳酸钙的质量为x,生成氯化钙的质量为y,生成二氧化碳的质量为... 在反应2A+5B=2C+4D中,C、D的相对分子质量之比为9 : 22。若2.6 gA与B完全反应后,生成8.8 gD。则在此反应中,B与D的质量比为 ( )
A. 4 : 9 B. 8 : 11 C. 10 : 11 D. 31 : 44
 C
【解析】
试题利用C、D的相对分子质量之比及反应中C、D物质的分子个数关系,可计算出反应中这两种物质的质量比;再根据C、D物质的质量关系,由生成D的质量,可计算出生成C物质的质量;最后使用质量守恒定律,求得参加反应的B物质的质量,从而计算出B与D的质量比。
设生成8.8gD,同时生成C的质量为x,
2A + 5B = 2C + 4D
2×9 4×22
x 8...
C
【解析】
试题利用C、D的相对分子质量之比及反应中C、D物质的分子个数关系,可计算出反应中这两种物质的质量比;再根据C、D物质的质量关系,由生成D的质量,可计算出生成C物质的质量;最后使用质量守恒定律,求得参加反应的B物质的质量,从而计算出B与D的质量比。
设生成8.8gD,同时生成C的质量为x,
2A + 5B = 2C + 4D
2×9 4×22
x 8... 某些饮料中常溶解一定量的二氧化碳,溶解在水中的一部分二氧化碳与水反应生成碳酸,所以这种饮料也称为碳酸饮料.
(1)分析上述信息,归纳出二氧化碳的一点物理性质________
(2)碳酸的化学式为H2CO3,碳酸是由________ 元素组成的
(3)二氧化碳中,碳元素与氧元素的质量比为________
 二氧化碳能溶于水氢、碳、氧3:8.
【解析】
(1)根据题干信息可以看出,二氧化碳能够溶于水;(2)根据碳酸的化学式可以看出,碳酸含有氢、碳和氧三种元素;(3)二氧化碳中,碳元素和氧元素的质量比是12:(16?3)=3:8。
二氧化碳能溶于水氢、碳、氧3:8.
【解析】
(1)根据题干信息可以看出,二氧化碳能够溶于水;(2)根据碳酸的化学式可以看出,碳酸含有氢、碳和氧三种元素;(3)二氧化碳中,碳元素和氧元素的质量比是12:(16?3)=3:8。 向盛有紫色石蕊试液的试管中通入适量的CO2,紫色石蕊试液的试液变为红色,其反应的化学方程式为________________.将反应后的溶液加热,则石蕊由红色变为紫色,其反应的化学方程式为_________________.
 CO2十H2O=H2CO3H2CO3=CO2↑+H2O
【解析】
CO2能溶于水并与水反应生成碳酸,使紫色石蕊试液变成红色:CO2十H2O=H2CO3.H2CO3又是一种不稳定的酸,易分解重新放出CO2,使试液又由红色变成紫色:H2CO3=CO2↑+H2O;
故答案为:CO2+H2O=H2CO3. H2CO3═CO2↑+H2O.
CO2十H2O=H2CO3H2CO3=CO2↑+H2O
【解析】
CO2能溶于水并与水反应生成碳酸,使紫色石蕊试液变成红色:CO2十H2O=H2CO3.H2CO3又是一种不稳定的酸,易分解重新放出CO2,使试液又由红色变成紫色:H2CO3=CO2↑+H2O;
故答案为:CO2+H2O=H2CO3. H2CO3═CO2↑+H2O. 葡萄糖是生命活动中不可缺少的物质
A. 无色晶体或白色粉末 B. 葡萄糖在人体内能被氧气氧化为二氧化碳和水
C. 密度为1.544g/cm3,熔点为146℃ D. 易溶于水,微溶于乙醇,不溶于乙醚
 B
【解析】
试题物理性质包括物质的颜色、状态、气味、密度、熔点、沸点、溶解性等。化学性质包括可燃性、还原性、氧化性等。故属于葡萄糖化学性质的是B。
B
【解析】
试题物理性质包括物质的颜色、状态、气味、密度、熔点、沸点、溶解性等。化学性质包括可燃性、还原性、氧化性等。故属于葡萄糖化学性质的是B。 实验结束后,下列仪器的放置方法正确的是( )

A. A B. B C. C D. D
 D
【解析】
试题使用后的胶头滴管不能平放在试验台上,防止腐蚀桌面、或污染试剂或腐蚀胶帽;取完试剂后应及时盖上瓶盖,标签向外放回原处;用完托盘天平后,应将砝码放回砝码盒,并将游码归零。
D
【解析】
试题使用后的胶头滴管不能平放在试验台上,防止腐蚀桌面、或污染试剂或腐蚀胶帽;取完试剂后应及时盖上瓶盖,标签向外放回原处;用完托盘天平后,应将砝码放回砝码盒,并将游码归零。 
