题目内容
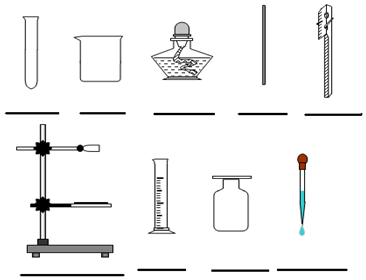
10.某同学在用天平称量物体时重32.6g,称完时他发现物码放反了,但他仍然得到了准确的结果(5g 以下用游码)( )| A. | 32.6g | B. | 31.4 g | C. | 27.4g | D. | 必须重称 |
分析 根据天平的使用方法是左物右码,左盘的质量等于右盘的质量加游码的质量,即药品质量=砝码质量+游码质量,如果位置放反,根据左盘的质量=右盘的质量+游码的质量,列等式进行计算.
解答 解:由左盘的质量=右盘的质量+游码的质量可知:砝码质量=物品质量+游码的质量,所以物品质量=砝码质量-游码质量,即该同学称取药品的实际质量为:30g-2.6g=27.4g.
烧杯的真实质量=30g-2.6g=27.4g.
故选:C.
点评 本题考查了对托盘天平的使用,掌握左盘质量=右盘质量+游码质量是解题的关键.

练习册系列答案
相关题目
20.下列关于合金的说法正确的是( )
| A. | 合金不能传热、导电 | |
| B. | 合金的熔点较组成合金的金属都高 | |
| C. | 合金的很多性能与组成其纯金属不同 | |
| D. | 合金没有延展性 |
1.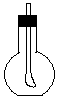 用如图装置做趣味实验:在用胶塞塞紧的烧瓶里充满某种气体(X),烧瓶内导管的一端事先已绑好了一个气球.拔开胶塞,迅速倒入另一种溶液(Y),再立即塞紧胶塞,振荡,此时可以看到气球逐渐膨胀的是( )
用如图装置做趣味实验:在用胶塞塞紧的烧瓶里充满某种气体(X),烧瓶内导管的一端事先已绑好了一个气球.拔开胶塞,迅速倒入另一种溶液(Y),再立即塞紧胶塞,振荡,此时可以看到气球逐渐膨胀的是( )
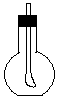 用如图装置做趣味实验:在用胶塞塞紧的烧瓶里充满某种气体(X),烧瓶内导管的一端事先已绑好了一个气球.拔开胶塞,迅速倒入另一种溶液(Y),再立即塞紧胶塞,振荡,此时可以看到气球逐渐膨胀的是( )
用如图装置做趣味实验:在用胶塞塞紧的烧瓶里充满某种气体(X),烧瓶内导管的一端事先已绑好了一个气球.拔开胶塞,迅速倒入另一种溶液(Y),再立即塞紧胶塞,振荡,此时可以看到气球逐渐膨胀的是( )| 选项 | X | Y |
| A | 氧气 | 澄清石灰水 |
| B | 氯化氢 | 氢氧化钾溶液 |
| C | 二氧化碳 | 盐酸溶液 |
| D | 二氧化碳 | 氢氧化钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
19.能一次性鉴别氧气、氮气和空气三瓶气体的简便方法是( )
| A. | 看颜色闻气味 | B. | 用燃着的木条 | C. | 称质量比密度 | D. | 用带火星的木条 |
20.某同学查阅资料得知,实验室常用电石(主要成分CaC2)与水反应制取乙炔(C2H2),反应的化学方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑(电石中的杂质不溶于水且不与水反应,也不与Na2CO3反应).在实验室中,该同学把一定量的CaC2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液,并对滤液的成分进行探究.
〔提出问题〕:滤液中溶质的成分是什么?
〔猜想与假设〕:猜想一:NaOH、Na2CO3
猜想二:NaOH
猜想三:NaOH、Ca(OH)2
[分析与推理]:
分析一:若猜想一成立,说明实验中加入的CaC2量少,CaC2与水反应生成的Ca(OH)2与Na2CO3反应后,Na2CO3剩余.
分析二:若猜想二成立,说明实验中加入的CaC2与水反应生成的Ca(OH)2与Na2CO3恰好完全反应后.
分析三:若猜想三成立,说明实验中加入的CaC2量多,CaC2与水反应生成的Ca(OH)2与Na2CO3反应后,Ca(OH)2剩余.
由以上分析可推知:反应后滤液中一定存在的溶质是NaOH(填化学式,下同),可能存在的溶质是Na2CO3和Ca(OH)2.对可能存在的溶质,需要进一步实验验证.
[设计并实验]
[拓展延伸]
若向CuCl2溶液中加入少量CaC2,充分反应,可观察到有气泡产生,同时出现蓝色的Cu(OH)2(填化学式)沉淀.
实验室保存电石应注意放在干燥处.
〔提出问题〕:滤液中溶质的成分是什么?
〔猜想与假设〕:猜想一:NaOH、Na2CO3
猜想二:NaOH
猜想三:NaOH、Ca(OH)2
[分析与推理]:
分析一:若猜想一成立,说明实验中加入的CaC2量少,CaC2与水反应生成的Ca(OH)2与Na2CO3反应后,Na2CO3剩余.
分析二:若猜想二成立,说明实验中加入的CaC2与水反应生成的Ca(OH)2与Na2CO3恰好完全反应后.
分析三:若猜想三成立,说明实验中加入的CaC2量多,CaC2与水反应生成的Ca(OH)2与Na2CO3反应后,Ca(OH)2剩余.
由以上分析可推知:反应后滤液中一定存在的溶质是NaOH(填化学式,下同),可能存在的溶质是Na2CO3和Ca(OH)2.对可能存在的溶质,需要进一步实验验证.
[设计并实验]
| 实验序号 | 实验操作 | 实验现象 | 实验结论 |
| 实验一 | 取少量滤液于试管中,向其中加入过量稀盐酸 | 无气泡产生 | 猜想一不成立 |
| 实验二 | 另取少量滤液于试管中,向其中滴入适量碳酸钠溶液 | 产生白色沉淀 | 猜想三成立,发生反应的化学方程式为 Ca(OH)2+Na2CO3=CaCO3+2NaOH |
若向CuCl2溶液中加入少量CaC2,充分反应,可观察到有气泡产生,同时出现蓝色的Cu(OH)2(填化学式)沉淀.
实验室保存电石应注意放在干燥处.