题目内容
4.硼烷的结构像鸟巢,故称为巢式硼烷.五硼烷(B5H9)为传统火箭燃料,燃烧产物对环境污染小.下图是三种巢式硼烷,下列说法正确的是( )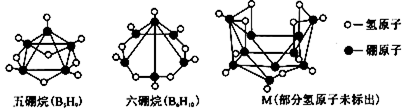
| A. | 六硼烷由6个硼原子和10个氢原子构成 | |
| B. | 图中M的名称为九硼烷 | |
| C. | 硼烷有可能是未来的清洁能源 | |
| D. | 2B5H9+12O2$\frac{\underline{\;点燃\;}}{\;}$5X+9H2O,则X中B的化合价为+5价 |
分析 A.根据物质的结构来分析;
B.根据物质的结构以及化合物的命名方法来分析;
C.根据硼烷燃烧产物对环境污染小的特点,推断硼烷的用途;
D.由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式;由在化合物中正负化合价代数和为零,进行分析判断.
解答 解:A.六硼烷是由六硼烷分子构成的,每个六硼烷分子是由6个硼原子和10个氢原子构成,故错误;
B.由如图所示前两种巢式硼烷的化学式可知,五硼烷、六硼烷的1个分子中分别含有5、6个碳原子,图中M的1个分子中含有9个碳原子,则图中M的名称为九硼烷,故错误;
C.由于硼烷燃烧产物对环境污染小,因此硼烷有可能成为未来的清洁能源;故正确;
D.反应后的生成物中硼、氢、氧原子个数分别为0、18、9,根据反应前后原子种类、数目不变,则5X中含有10个硼原子和15个氧原子,则每个X分子由1个硼原子和3个氧原子构成,则物质X的化学式为BO3;氧元素显-2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×3=0,则x=+6价,故错误.
故选C.
点评 本题难度不大,推导出巢式硼烷的通式和命名方法、原子守恒来确定物质的化学式、利用化合价的原则计算指定元素的化合价的方法是正确解答本题的关键.

练习册系列答案
相关题目
17.下列实验方案的设计中,没有正确体现对比这种科学思想的是( )
| A. | 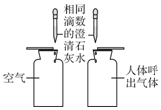 比较二氧化碳的含量 | B. | 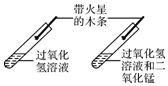 研究二氧化锰的催化作用 | ||
| C. | 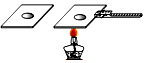 研究蒸发快慢影响的因素 | D. | 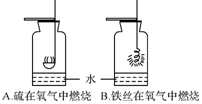 实验中水的作用 |
18.下列实验操作或装置正确的是( )
| A. | 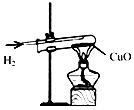 氢气还原氧化铜 氢气还原氧化铜 | B. | 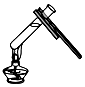 加热液体 | C. | 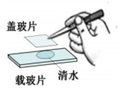 盖盖玻片 | D. |  使用测电笔 |
12.下列化学实验操作顺序正确的是( )
| A. | 氢气还原氧化铜实验中,当氧化铜全部被还原时,先停止通氢气再熄灭酒精灯 | |
| B. | 在精盐提纯实验中,将粗盐溶于水后先加热蒸发再进行过滤 | |
| C. | 加热高锰酸钾制取氧气,用排水法集满氧气后先从水槽中移出导管再熄灭酒精灯 | |
| D. | 用氯酸钾和二氧化锰混合物制取氧气时,先装药品再检验装置的气密性 |
13.一瓶未贴标签的粉末状常见金属R.为测定R的相对原子质量,准确称取一定量该金属粉末,在坩埚内加强热使其完全氧化,冷却后再称重.重复实验,获得如表数据.请回答:
(1)表格中m=85.0.
(2)已知R的化合价为+3价,则R的相对原子质量为27.
(3)若用该金属与稀硫酸反应制取0.6克氢气,至少需要质量分数为10%的稀硫酸溶液多少克?
| 实验次数 | 金属质量(g) | 金属氧化物质量(g) |
| l | 45.0 | 84.9 |
| 2 | 45.0 | 85.1 |
| 3 | 45.0 | 85.0 |
| 平均值 | 45.0 | m |
(2)已知R的化合价为+3价,则R的相对原子质量为27.
(3)若用该金属与稀硫酸反应制取0.6克氢气,至少需要质量分数为10%的稀硫酸溶液多少克?
14.为了除去物质中的杂质(括号内为杂质),所选试剂(适量)及操作方法均正确的是( )
| 物 质 | 选用试剂(适量) | 操作方法 | |
| A | Cu(CuO) | 氧气 | 通入氧气并加热 |
| B | CO2(HCl) | 氢氧化钠溶液 | 气体通过盛有氢氧化钠溶液的洗气瓶 |
| C | NaOH(Na2CO3) | 稀盐酸 | 加入稀盐酸充分反应 |
| D | KCl溶液(K2CO3) | 氯化钙溶液 | 加入氯化钙溶液充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
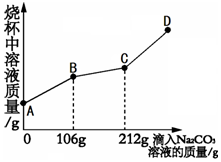 在一烧杯中盛有l00克BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示,请根据题意问答问题:
在一烧杯中盛有l00克BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示,请根据题意问答问题: