题目内容
某溶液里滴入氯化钡溶液后产生不溶于稀硝酸的白色沉淀,则此白色沉淀( )
| A、一定是硫酸钡 |
| B、一定是碳酸钡 |
| C、一定氯化银 |
| D、是硫酸钡或氯化银 |
考点:盐的化学性质
专题:常见的盐 化学肥料
分析:从“银离子和氯离子结合生成的氯化银、硫酸根离子和钡离子结合生成的硫酸钡都是不溶于稀硝酸的白色沉淀”进行分析、解答.
解答:解:氯化钡会电离出Cl-和Ba2+.
若向其中加入含有Ag+的溶液,则会产生不溶于稀硝酸的氯化银白色沉淀,
若向其中加入含SO42-的溶液,也会产生不溶于稀硝酸的硫酸钡白色沉淀;
所以,该溶液中可能含有硫酸根离子或银离子,即该白色沉淀是硫酸钡或氯化银.
故选:D.
若向其中加入含有Ag+的溶液,则会产生不溶于稀硝酸的氯化银白色沉淀,
若向其中加入含SO42-的溶液,也会产生不溶于稀硝酸的硫酸钡白色沉淀;
所以,该溶液中可能含有硫酸根离子或银离子,即该白色沉淀是硫酸钡或氯化银.
故选:D.
点评:检验硫酸根的方法是:先向其中加入盐酸酸化,若无白色沉淀生成,再加氯化钡溶液,若有白色沉淀生成,则证明有硫酸根离子;
检验氯离子的方法是:向其中加入硝酸酸化的硝酸银溶液,若有白色沉淀生成,则证明有氯离子.
检验氯离子的方法是:向其中加入硝酸酸化的硝酸银溶液,若有白色沉淀生成,则证明有氯离子.

练习册系列答案
相关题目
下列气体中可用固体氢氧化钠做干燥剂的是( )
| A、氯化氢 | B、氢气 |
| C、二氧化碳 | D、二氧化硫 |
下列物质能够反应,但没有明显现象的是( )
| A、硫酸铜溶液中加入氢氧化钠 |
| B、碳酸钠溶液加入澄清石灰水中 |
| C、稀盐酸滴入澄清石灰水 |
| D、氯化镁溶液中滴入硫酸铜溶液 |
下列说法,正确的是( )
| A、1g食盐完全溶解在100g水中,得到溶质质量分数为1%食盐水溶液 |
| B、把1g面粉放入100g水里搅拌,得到101g 面粉水溶液 |
| C、10mL酒精与20mL水混合后,得到30mL酒精水溶液 |
| D、把1滴植物油滴入10mL汽油中充分振荡,可以得到溶液 |
不属于酸、碱、盐的物质是( )
| A、HNO3 |
| B、NH4HCO3 |
| C、NH3?H2O |
| D、NO2 |
一个密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得数据见下表.下列说法中正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量 | 10g | 35g | 10g | 12g |
| 反应后质量 | 4g | X | 10g | 46g |
| A、X=7g |
| B、在该反应中,丙物质一定做催化剂 |
| C、该反应是分解反应 |
| D、反应中反应物甲和丁的质量比为3:17 |
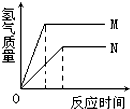 等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述不正确的是( )
等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述不正确的是( )| A、M、N两种金属中较活泼的是M |
| B、生成H2的质量M>N |
| C、相对原子质量较大的是M |
| D、产生H2的速率M>N |
用判断镁条在氧气中燃烧发生了化学变化的主要依据是( )
| A、剧烈燃烧 |
| B、耀眼的强光 |
| C、放出大量的热 |
| D、生成一种白色固体物质 |