题目内容
5.若3.2g某物质在空气中完全燃烧生成4.4g二氧化碳和3.6g水,则下列描述不正确的是( )| A. | 该物质只含有碳元素和氢元素 | |
| B. | 该物质中碳元素与氢元素的质量比为3:1 | |
| C. | 该物质中碳原子与氢原子的个数比为1:4 | |
| D. | 该物质燃烧消耗氧气的质量为4.8g |
分析 根据质量守恒定律,由生成物可以初步确定该物质中含有氢元素和氧元素,由生成的二氧化碳和水中碳、氢元素的质量和与该物质的质量进行对比,从而确定该物质的组成元素;据此进行分析判断.
解答 解:4.4gCO2中含有碳元素的质量为:4.4g×$\frac{12}{44}$100%=1.2g,3.6g水中含有氢元素的质量为:3.6g×$\frac{2}{18}$×100%=0.4g,生成物4.4g二氧化碳和3.6g水所含碳、氢元素的质量和=1.2g+0.4g=1.6g,小于该物质的质量,则该物质中一定含有碳、氢、氧三种元素.
A、由上述分析可知,该物质一定含有碳、氢、氧三种元素,故选项说法错误.
B、由上述分析可知,该物质中碳元素与氢元素的质量比为1.2g:0.4g=3:1,故选项说法正确.
C、该物质的分子中碳原子与氢原子的个数比为$\frac{1.2g}{12}$:$\frac{0.4g}{1}$=1:4,故选项说法正确.
D、该物质燃烧消耗氧气的质量为:4.4g+3.6g-3.2g=4.8g,正确.
故选A.
点评 本题难度稍大,主要考查了质量守恒定律、化学式的计算,解题的关键是根据质量守恒定律确定确定物质的元素组成.

练习册系列答案
相关题目
6.“雪碧”是一种无色的碳酸饮料,将少量“雪碧”滴入紫色石蕊试液中,然后加热,溶液颜色的变化是( )
| A. | 先变红后变紫 | B. | 变红后颜色不再改变 | ||
| C. | 先变蓝后变紫 | D. | 先变红色后变无色 |
17.下列材料属于天然材料的是( )
| A. | 羊毛 | B. | 钢铁 | C. | 玻璃 | D. | 食品保鲜膜 |
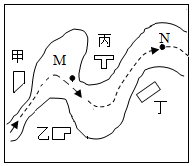 某中学环保监测小组的同学在一条鱼虾绝迹的小河边发现四所工厂,如图.这些工厂向小河所排放的废水中各含一种化合物,经检测发现:①甲处河水呈黄色;②乙处河水呈红褐色浑浊状;③丙处河水变澄清;④丁处河水不断冒气泡;⑤M处水样PH>7,加足量HNO3再加BaCl2溶液后无沉淀;⑥N处水样PH<7.?
某中学环保监测小组的同学在一条鱼虾绝迹的小河边发现四所工厂,如图.这些工厂向小河所排放的废水中各含一种化合物,经检测发现:①甲处河水呈黄色;②乙处河水呈红褐色浑浊状;③丙处河水变澄清;④丁处河水不断冒气泡;⑤M处水样PH>7,加足量HNO3再加BaCl2溶液后无沉淀;⑥N处水样PH<7.?