题目内容
8.农业兴趣小组同学需要溶质质量分数为15%的氯化钠溶液进行选种.但实验恰好无15%的氯化钠溶液剩余,只有几瓶饱和的氯化钠溶液(密度为ρ1)和几瓶溶质质量分数为10%的氯化钠溶液(密度为ρ2).请帮农业兴趣小组同学配制合适浓度的溶液进行选种.已知:室温为20℃,该温度下氯化钠的溶解度为36克.
(1)室温为20℃时氯化钠饱和溶液的溶质质量分数为26.5%
(2)实验仪器:除了烧杯之外,实验中还需要的玻璃仪器有量筒、玻璃棒(写出两种)
(3)若取用饱和溶液的体积为V1,取用10%的氯化钠溶液的体积为V2则利用题目所给数据计算:V1:V2的数学表达式:$\frac{20{ρ}_{2}}{53{ρ}_{1}}$
(4)简要说明实验步骤.
分析 (1)根据20℃时,氯化钠饱和溶液的溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%进行解答.
(2)根据配制一定溶质质量分数的溶液所需的仪器解答;
(3)根据溶液稀释前后溶质质量不变进行分析.
(4)根据配制溶液的步骤:计算、称量、溶解进行分析;
解答 解:
(1)室温为20℃时,氯化钠饱和溶液的溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%=$\frac{36g}{36g+100g}$×100%=26.5%.
(2)实验仪器:除了烧杯之外,实验中还需要的玻璃仪器量筒、玻璃棒、胶头滴管;
(3)根据溶液稀释前后溶质质量不变,
V1ρ126.5%=V2ρ210%
V1:V2的数学表达式:$\frac{{ρ}_{2}10%}{{ρ}_{1}26.5%}$=$\frac{20{ρ}_{2}}{53{ρ}_{1}}$
(4)配制溶液的步骤是:先计算再量取最后溶解,装瓶存放.
答案:
(1)26.5%;
(2)量筒、玻璃棒;
(3)$\frac{20{ρ}_{2}}{53{ρ}_{1}}$
(4)先计算再量取最后溶解,装瓶存放.
点评 熟练掌握配制溶液的步骤,仪器,溶质的质量分数计算是解答此题的基础和关键.

练习册系列答案
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
18.2013年3月底,上海、安徽等地出现H7N9新型流感病毒,严重威胁了人们的健康,其治疗的有效药物达菲可用莽草酸(C7H10O5)制取.有关莽草酸的说法正确的是( )
| A. | 莽草酸中氢元素的质量分数最大 | B. | 莽草酸由碳、氢、氧三种元素组成 | ||
| C. | 莽草酸中各元素的质量比为7:10:5 | D. | 每个莽草酸分子里含有5个氢分子 |
19.如图所示取用试剂的操作图示正确的是( )
| A. |  称量固体 | B. | 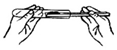 用纸槽取用粉末 | C. | 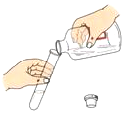 倾倒液体 | D. |  过滤 |