题目内容
3.某同学设计一氧化碳还原氧化铜的实验如图所示,下列说法错误的是( )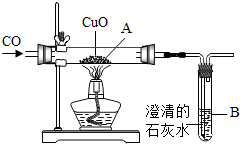
| A. | 实验开始时,要先通一氧化碳,再给A处的氧化铜加热 | |
| B. | 通过观察黑色固体颜色的变化判断反应是否发生 | |
| C. | 该装置设计方案合理无需改进 | |
| D. | 实验结束后,要先熄灭酒精灯 |
分析 一氧化碳还原氧化铜的实验步骤是:‘一氧化碳早出晚归,酒精灯迟到早退’,即实验开始先通入一氧化碳,然后加热氧化铜,由黑变红先撤灯,继续通入一氧化碳至试管冷却,同时要注意尾气的处理.
解答 解:A、实验开始先通入一氧化碳,然后加热氧化铜,目的是排尽试管内空气,防止发生爆炸,正确;
B、由于一氧化碳具有还原性能将氧化铜还原为红色的铜,通过观察黑色固体颜色的变化判断反应是否发生,故正确;
C、一氧化碳有毒,故反应尾气要处理,防止排放到空气中污染空气,所以该装置设计方案不合理需改进,故错误;
D、反应结束要先熄灭酒精灯,继续通入一氧化碳至试管冷却,防止生成的铜在较高温度下被氧化,正确.
故选C.
点评 了解一氧化碳还原氧化铜的实验步骤及操作的原理,一氧化碳的性质即可顺利解答.

练习册系列答案
相关题目
16.垃圾分类从我做起,金属饮料罐属于( )
| A. |  可回收物 | B. |  有害垃圾 | C. |  厨余垃圾 | D. |  其他垃圾 |
14.我们生活在不断变化的物质世界中,下列变化属于物理变化的是( )
| A. | 蜡烛的燃烧 | B. | 二氧化碳使澄清石灰水变浑浊 | ||
| C. | 铁钉在潮湿的空气中生锈 | D. | 直饮水机中活性炭吸附杂质 |
11.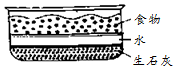 “自热饭盒”是一种使用化学方法加热的方便食品,也就是将盒饭下面的拉条拉出,饭菜便可以自动加热.关于自热饭盒,下列说法正确的是( )
“自热饭盒”是一种使用化学方法加热的方便食品,也就是将盒饭下面的拉条拉出,饭菜便可以自动加热.关于自热饭盒,下列说法正确的是( )
 “自热饭盒”是一种使用化学方法加热的方便食品,也就是将盒饭下面的拉条拉出,饭菜便可以自动加热.关于自热饭盒,下列说法正确的是( )
“自热饭盒”是一种使用化学方法加热的方便食品,也就是将盒饭下面的拉条拉出,饭菜便可以自动加热.关于自热饭盒,下列说法正确的是( )| A. | 生石灰和水反应会吸收热量 | |
| B. | 自热饭盒利用的是生石灰的内能 | |
| C. | 自热饭盒在加热过程中内能增加 | |
| D. | 加热后盒子内壁上出现小水珠,这是熔化现象 |
8. 开化龙顶茶产于衢州市开化县齐溪乡白云山(如图).茶叶中的咖啡因能使中枢神经系统兴奋,因此能够增加警觉度,使人警醒,有快速而清晰的思维,增加注意力和保持较好的身体状态.咖啡因的化学式为C8H10N4O2,则关于咖啡因的说法中错误的是( )
开化龙顶茶产于衢州市开化县齐溪乡白云山(如图).茶叶中的咖啡因能使中枢神经系统兴奋,因此能够增加警觉度,使人警醒,有快速而清晰的思维,增加注意力和保持较好的身体状态.咖啡因的化学式为C8H10N4O2,则关于咖啡因的说法中错误的是( )
 开化龙顶茶产于衢州市开化县齐溪乡白云山(如图).茶叶中的咖啡因能使中枢神经系统兴奋,因此能够增加警觉度,使人警醒,有快速而清晰的思维,增加注意力和保持较好的身体状态.咖啡因的化学式为C8H10N4O2,则关于咖啡因的说法中错误的是( )
开化龙顶茶产于衢州市开化县齐溪乡白云山(如图).茶叶中的咖啡因能使中枢神经系统兴奋,因此能够增加警觉度,使人警醒,有快速而清晰的思维,增加注意力和保持较好的身体状态.咖啡因的化学式为C8H10N4O2,则关于咖啡因的说法中错误的是( )| A. | 咖啡因的相对分子质量为194 | |
| B. | 咖啡因由碳、氢、氧、氮四种元素组成 | |
| C. | 咖啡因中碳、氢、氮、氧元素的质量比为4:5:2:1 | |
| D. | 咖啡因属于有机化合物 |
15.已知某金属粉末中除含有Al外还含有一定量的Fe,为测定金属的含量,某化学兴趣小组的同学展开了如下的实验探究.
小资料:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:
2Al+2H2O+2NaOH═2NaAlO2+3H2↑,Fe不与氢氧化钠溶液反应).
取20g该金属粉末,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据如下:
(1)第四次加入NaOH后,溶液中的溶质是氢氧化钠和偏铝酸钠;
(2)Fe的质量分数为30%;
(3)第三次加入氢氧化钠溶液后,共生成多少克氢气?所用氢氧化钠溶液的溶质质量分数为多少?(精确到0.1%)
小资料:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:
2Al+2H2O+2NaOH═2NaAlO2+3H2↑,Fe不与氢氧化钠溶液反应).
取20g该金属粉末,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据如下:
| 加NaOH溶液的次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 剩余固体的质量/g | 16.4 | 12.8 | 9.2 | 6 | m |
(2)Fe的质量分数为30%;
(3)第三次加入氢氧化钠溶液后,共生成多少克氢气?所用氢氧化钠溶液的溶质质量分数为多少?(精确到0.1%)
12.下列现象和应用中,所包含的主要变化有一项与其他三项有本质区别,该项是( )
| A. | 黄豆霉变 | |
| B. | 酸雨腐蚀铁制栏杆 | |
| C. | 利用熟石灰改良酸性土壤 | |
| D. | 利用沸点不同分离液态空气制得氧气 |
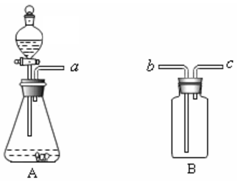 如图实验装置适当组合可用于O2、H2、CO2等气体的制备和收集.
如图实验装置适当组合可用于O2、H2、CO2等气体的制备和收集.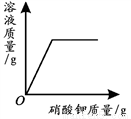 一定温度下,向不饱和硝酸钾溶液中加入硝酸钾
一定温度下,向不饱和硝酸钾溶液中加入硝酸钾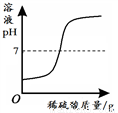 向一定量NaOH溶液中加入稀H2SO4
向一定量NaOH溶液中加入稀H2SO4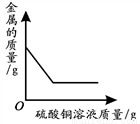 向一定量铁粉和铜粉的混合物中加入硫酸铜溶液
向一定量铁粉和铜粉的混合物中加入硫酸铜溶液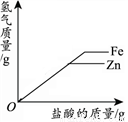 向相同质量的锌粉和铁粉中,分别加入足量的稀盐酸
向相同质量的锌粉和铁粉中,分别加入足量的稀盐酸